
9 يوليو، 2014
النتائج الجديدة تخفف من المخاوف السابقة من أن تقنيات تحرير الجينات - المستخدمة لتطوير علاجات للأمراض الجينية - يمكن أن تضيف طفرات غير مرغوب فيها إلى الخلايا الجذعية.
النتائج الجديدة تخفف من المخاوف السابقة من أن تقنيات تحرير الجينات - المستخدمة لتطوير علاجات للأمراض الجينية - يمكن أن تضيف طفرات غير مرغوب فيها إلى الخلايا الجذعية.
لا جولا - إن القدرة على تبديل جين بآخر في سلسلة من الخلايا الجذعية الحية قد انتقلت فقط من الخيال العلمي إلى الواقع خلال هذا العقد. كما هو الحال مع أي تقنية جديدة ، فإنها تجلب معها الأمل - الأمل في إصلاح الجينات المسببة للأمراض لدى البشر ، على سبيل المثال - بالإضافة إلى الأسئلة والمخاوف المتعلقة بالسلامة. الآن ، وضع علماء Salk أحد هذه المخاوف للراحة: استخدام تقنيات تعديل الجينات على الخلايا الجذعية لا يزيد من التكرار الكلي للطفرات في الخلايا. تم نشر النتائج الجديدة في 3 يوليو 2014 في المجلة خلية الخلايا الجذعية.
"القدرة على التعديل الدقيق للحمض النووي للخلايا الجذعية قد سرعت بشكل كبير من البحث عن الأمراض البشرية والعلاج بالخلايا" ، كما يقول كبير المؤلفين خوان كارلوس إيزبيسوا بيلمونتي، أستاذ في Salk's معمل التعبير الجيني. "لترجمة هذه التكنولوجيا بنجاح إلى العيادة ، نحتاج أولاً إلى فحص سلامة هذه الخلايا الجذعية المعدلة ، مثل استقرار الجينوم والحمل الطفري."
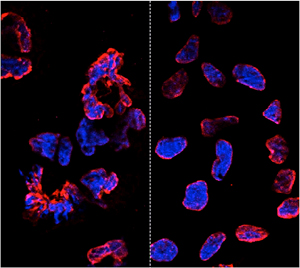
تظهر الدراسة الجديدة أن تقنيات تعديل الجينات خاصة بأهدافها ولا تقدم طفرات ضارة ، مما يمهد الطريق لتطوير علاجات آمنة في العيادة. تُظهر اللوحة اليسرى مغلفات نووية مشوهة (حمراء) من خلايا جذعية مستحثة متعددة القدرات مشتقة من خلايا مصابة بمرض باركنسون (الحمض النووي باللون الأزرق). تُظهر اللوحة اليمنى الخلايا المستحثة بالمثل والتي تم تحريرها جينيًا لاستعادة الخلايا.
اضغط هنا للحصول على صورة عالية الدقة.
الصورة: بإذن من معهد سالك للدراسات البيولوجية
عندما يرغب العلماء في تغيير تسلسل امتداد من الحمض النووي داخل الخلايا - إما لأغراض البحث أو لإصلاح طفرة جينية لأغراض علاجية - فإن لديهم خيارًا من طريقتين. يمكنهم استخدام فيروس مُعدّل هندسيًا لإيصال الجين الجديد إلى الخلية ؛ ثم تدمج الخلية تسلسل الحمض النووي الجديد بدلاً من التسلسل القديم. أو يمكن للعلماء استخدام ما يُعرف باسم نوكليازات مستهدفة مخصصة ، مثل بروتينات TALEN ، التي تقطع الحمض النووي في أي مكان مرغوب فيه. يمكن للباحثين استخدام البروتينات لقطع الجين الذي يريدون استبداله ، ثم إضافة جين جديد إلى المزيج. ستلصق آليات الإصلاح الطبيعية للخلية الجين الجديد في مكانه.
سابقًا ، كان مختبر بلمونتي رائدًا في استخدام الفيروسات المعدلة ، والتي تسمى ناقلات الفيروسات الغدية المعتمدة على المساعد (HDAdVs) تصحيح الطفرة الجينية التي تسبب مرض فقر الدم المنجلي، أحد أخطر أمراض الدم في العالم. استخدم هو وزملاؤه HDAdVs لاستبدال الجين المتحور في سلسلة من الخلايا الجذعية بنسخة خالية من الطفرات ، وإنشاء خلايا جذعية يمكن نظريًا أن تُغرس في نخاع عظام المرضى حتى تخلق أجسامهم خلايا دم صحية.
قبل تطبيق هذه التقنيات على البشر ، أراد باحثون مثل بلمونتي معرفة ما إذا كانت هناك مخاطر لتحرير الجينات في الخلايا الجذعية. على الرغم من أن تقنيات تحرير الجينات الشائعة أثبتت دقتها في تغيير الامتداد الصحيح للحمض النووي ، فإن العلماء قلقون من أن هذه العملية يمكن أن تجعل الخلايا أكثر استقرارًا وعرضة لطفرات في جينات غير مرتبطة - مثل تلك التي يمكن أن تسبب سرطان.
يقول مو لي ، زميل ما بعد الدكتوراه في مختبر بلمونتي ومؤلف الورقة الجديدة: "أثناء إعادة برمجة الخلايا إلى خلايا جذعية ، تميل إلى تراكم العديد من الطفرات". "لذلك يشعر الناس بطبيعة الحال بالقلق من أن أي عملية تجريها مع هذه الخلايا في المختبر - بما في ذلك تعديل الجينات - قد تولد المزيد من الطفرات."

من اليسار: Juan Carlos Izpisua Belmonte و Keiichiro Suzuki و Mo Li من مختبر التعبير الجيني
اضغط هنا للحصول على صورة عالية الدقة.
الصورة: بإذن من معهد سالك للدراسات البيولوجية
لمعرفة ما إذا كان هذا هو الحال ، مجموعة Belmonte ، بالتعاون مع BGI و مبادئ السلوك معهد الفيزياء الحيوية ، الأكاديمية الصينية للعلوم في الصين، إلى سلالة من الخلايا الجذعية تحتوي على الجين المتحور الذي يسبب مرض فقر الدم المنجلي. قاموا بتحرير جينات بعض الخلايا باستخدام أحد تصميمي HDAdV ، وحرروا البعض الآخر باستخدام واحد من اثنين من بروتينات TALEN ، واحتفظوا ببقية الخلايا في المزرعة دون تعديلها. بعد ذلك ، قاموا بتسلسل الجينوم الكامل لكل خلية من التعديلات الأربعة وتجربة التحكم.
بينما اكتسبت جميع الخلايا مستوى منخفضًا من الطفرات الجينية العشوائية أثناء التجارب ، فإن الخلايا التي خضعت لتحرير الجينات - سواء من خلال HDAdV - أو النهج القائمة على TALEN - لم يكن لديها طفرات أكثر من الخلايا المحفوظة في المزرعة.
يقول Keiichiro Suzuki ، زميل ما بعد الدكتوراه في مختبر Belmonte ومؤلف الدراسة ، "لقد فوجئنا بسرور بالنتائج". اكتشف الناس آلاف الطفرات التي تم إدخالها أثناء إعادة برمجة iPSC. لقد وجدنا أقل من مائة نوع من أشكال النيوكليوتيدات الفردية في جميع الحالات ".
يضيف لي أن النتيجة لا تعني بالضرورة أنه لا توجد مخاطر متأصلة في استخدام الخلايا الجذعية مع الجينات المعدلة ، لكن عملية التعديل لا تجعل الخلايا الجذعية أقل أمانًا.
يقول: "لقد توصلنا إلى أن خطر حدوث طفرة لا يرتبط بطبيعته بتعديل الجينات". "تمثل هذه الخلايا نفس المخاطر مثل استخدام أي خلايا أخرى يتم التلاعب بها من أجل العلاج الخلوي أو الجيني." ويضيف أن ورقتين أخريين تم نشرهما في نفس العدد تدعمان نتائجهما (واحدة تلو الأخرى جامعة جونز هوبكنز واحد من جامعة هارفارد والمتعاونين).
تخطط مجموعة بلمونت لمزيد من الدراسات لمعالجة ما إذا كان إصلاح الجينات في أنواع الخلايا الأخرى ، باستخدام أساليب أخرى ، أو استهداف جينات أخرى يمكن أن يتسبب في حدوث طفرات غير مرغوب فيها بشكل أو بآخر. في الوقت الحالي ، يأملون في أن تشجع النتائج التي توصلوا إليها العاملين في هذا المجال على متابعة تقنيات تعديل الجينات كطريقة محتملة لعلاج الأمراض الوراثية في المستقبل.
الباحثون الآخرون في الدراسة هم جينغ كو ، أبريل غوبل ، إيمي أيزاوا ، روبا ديفي سوليغالا ، جيسيكا كيم ، نا يونغ كيم ، هسين كاي لياو ، كريس بينر ، وكونسيبسيون رودريغيز إستيبان من معهد سالك للدراسات البيولوجية. Chang Yu و Xiaotian Yao و Senwei Tang و Fan Zhang و Feng Chen و Yabin Jin و Yingrui Li من BGI ؛ وجينغ تشو ، وتينجتينج يوان ، وروتونج رن ، وشيولينج شو ، وغوانغ-هوي ليو من معهد الفيزياء الحيوية ، الأكاديمية الصينية للعلوم.
تم دعم العمل من قبل مؤسسة G. Harold and Leila Y. Mathers الخيريةأطلقت حملة ليونا م. وهاري بي هيلمسليأطلقت حملة مؤسسة جلينأطلقت حملة معهد كاليفورنيا للطب التجديديأطلقت حملة المعاهد الوطنية للصحةأطلقت حملة الأكاديمية الصينية للعلومأطلقت حملة مؤسسة بكين للعلوم الطبيعية، و برنامج آلاف المواهب الشابة في الصين.
عن معهد سالك للدراسات البيولوجية:
معهد سالك للدراسات البيولوجية هو أحد المؤسسات البحثية الأساسية البارزة في العالم ، حيث يقوم أعضاء هيئة التدريس المشهورون دوليًا بالتحقيق في أسئلة علوم الحياة الأساسية في بيئة فريدة وتعاونية وإبداعية. من خلال التركيز على الاكتشاف وتوجيه الأجيال القادمة من الباحثين ، يقدم علماء Salk مساهمات رائدة لفهمنا للسرطان والشيخوخة والزهايمر والسكري والأمراض المعدية من خلال دراسة علم الأعصاب وعلم الوراثة وبيولوجيا الخلايا والنباتات والتخصصات ذات الصلة.
تم الاعتراف بإنجازات أعضاء هيئة التدريس بالعديد من الأوسمة ، بما في ذلك جوائز نوبل والعضويات في الأكاديمية الوطنية للعلوم. تأسس المعهد في عام 1960 من قبل رائد لقاح شلل الأطفال جوناس سالك ، وهو مؤسسة مستقلة غير ربحية ومعلم معماري.
مكتب الاتصالات
هاتف: (858) 453-4100
اضغط@salk.edu