
May 15, 2009
Fehlende genomische „Zaunpfähle“ erklären inaktivierte Tumorsuppressorgene bei Brustkrebs
Fehlende genomische „Zaunpfähle“ erklären inaktivierte Tumorsuppressorgene bei Brustkrebs
La Jolla, Kalifornien – Unser Genom ist ein Flickenteppich aus Stadtteilen, die unterschiedlicher nicht sein könnten: In einigen Gegenden herrscht reges Treiben mit Genaktivitäten, während andere dünn besiedelt sind und ständig abgeriegelt sind. Laut Forschern des Salk Institute for Biological Studies verwischt das Durchbrechen einiger weniger molekularer Barrieren, die sie trennen, die Grenzen und führt zur Inaktivierung von mindestens zwei Tumorsuppressorgenen.
Ihre Ergebnisse wurden in der Ausgabe vom 15. Mai 2009 veröffentlicht Molekulare ZelleErklären Sie, wie ein einzelnes Ereignis eine Zelle auf dem Weg zur Tumorzelle weit voranbringen kann. „Das selektive Entfernen einiger Zaunpfähle löst eine Kaskade globaler Veränderungen im gesamten Genom aus, die schließlich zu Krebs führen können“, sagt er Beverly Emerson, Ph.D., Professor am Regulatory Biology Laboratory, der die Studie leitete.
Normalerweise wird die Zellvermehrung durch ein komplexes Netzwerk aus Beschleunigern (Wachstumsfaktoren) und Bremsen (Tumorsuppressoren) unter Kontrolle gehalten. Tumore entstehen, wenn Veränderungen im Genom krebserregende Gene aktivieren oder Tumorsuppressorgene inaktivieren, die dieses empfindliche Gleichgewicht zugunsten eines unkontrollierten Zellwachstums verschieben.
„Seit langer Zeit versucht man zu verstehen, wie Tumorsuppressorgene bei Krebs zum Schweigen gebracht werden“, sagt der Postdoktorand und Erstautor Michael Witcher. „Da wir nun eines der Schlüsselereignisse herausgefunden haben, das zu ihrer Inaktivierung führt, können wir diesen Mechanismus möglicherweise nutzen, um neuartige Therapien zu entwickeln.“
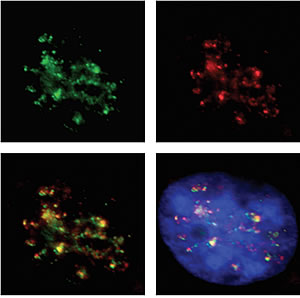
Oben links: Molekulare Zaunpfähle (grün dargestellt) trennen aktive von inaktiven chromosomalen Nachbarschaftsbereichen. Oben rechts: RNA-Polymerase 2 (rot dargestellt) liest Gene in aktiven Nachbarschaften. Unten links: Intakte Zäune befinden sich gemeinsam mit Bereichen mit Genaktivität. Überlappungsbereiche werden gelb angezeigt. Unten rechts: DNA ist blau dargestellt.
Bild: Mit freundlicher Genehmigung von Michael Witcher, Salk Institute for Biological Studies
Wenn die DNA einer einzelnen menschlichen Zelle ausgestreckt würde, würde sie einen sehr dünnen Faden von etwa 6 m Länge bilden. Damit ein so langes Molekül in den Zellkern passt und alles sauber organisiert bleibt, wird die DNA um Histonproteine gefädelt und in einer hochkondensierten Struktur namens Heterochromatin aufgerollt. In Bereichen der Genaktivität wird das dicht gepackte Chromatin gerade so weit entfaltet, dass die DNA für regulatorische Proteine zugänglich ist.
Bei vielen verschiedenen Krebsarten, einschließlich Brust-, Lungen-, Leber- und Bauchspeicheldrüsentumoren sowie multiplem Myelom und Lymphom, vergräbt sich der Tumorsuppressor p16 jedoch tief im Heterochromatin. Dadurch kann es von der Transkriptionsmaschinerie nicht gelesen werden und ist nicht in der Lage, das Zellwachstum zu überwachen.
Forscher wussten schon seit langem, dass p16 manchmal zum Schweigen gebracht wird, lange bevor eine Zelle krebsartig wird. Doch warum dieser bestimmte DNA-Abschnitt mit chemischen Markierungen gekennzeichnet war und so fest aufgewickelt wurde, dass er unzugänglich wurde, blieb ein Rätsel.
Die meisten Menschen suchten nach Hinweisen in der unmittelbaren Umgebung des Gens, wurden aber nicht fündig. Als Witcher seine Suche jedoch weiter flussaufwärts ausweitete, entdeckte er eine Bindungsstelle für CTCF, kurz für CCCTC-Bindungsfaktor, die das Herzstück der molekularen Zaunpfähle bildet, die Heterochromatin vom Rest des Genoms trennen. „Wir haben herausgefunden, dass die Bindung dieses Proteins an mehreren Bindungsstellen in zahlreichen Arten von Krebszellen verloren geht, was zum Zusammenbruch der molekularen Grenze führt“, sagt er. „Sobald die Grenze verschwunden war, drang das benachbarte Heterochromatin ein und brachte das nächstgelegene Gen zum Schweigen.“
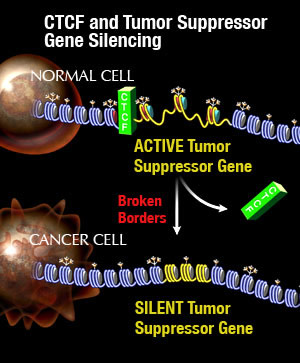
CTCF und Tumorsuppressor-Gen-Stummschaltung
Bild: Mit freundlicher Genehmigung von Jamie Simon, Salk Institute for Biological Studies
Weitere Experimente ergaben, dass CTCF fehlte, weil ihm eine chemische Modifikation namens „PARlation“ fehlte, Laborjargon für Poly(ADP-Ribosyl)ierung, die es dem Protein ermöglicht, an ausgewählte Stellen im Genom zu binden. „Ohne PARlation kann CTCF nicht den Komplex bilden, der zur Regulierung von p16 und des Tumorsuppressors RASSF1A und möglicherweise auch anderer erforderlich ist, was erklärt, warum Brustkrebszellen immer sowohl stillgelegtes p16 als auch stillgelegtes RASSF1A enthalten“, sagt Witcher.
„Wir glauben, dass die Destabilisierung spezifischer Chromosomengrenzen oder der Verlust molekularer Zäune durch eine fehlerhafte CTCF-Funktion ein allgemeiner Mechanismus zur Inaktivierung von Tumorsuppressorgenen und zur Einleitung der Tumorentstehung bei zahlreichen Formen menschlicher Krebsarten sein könnte“, sagt Emerson.
Für Informationen zur Kommerzialisierung dieser Technologie wenden Sie sich bitte an das Salk Office of Technology Development (858) 453-4100, Durchwahl. 1278.
Diese Arbeit wurde von der Samuel Waxman Cancer Research Foundation und dem Canadian Institute of Health Research unterstützt.
Über das Salk Institute for Biological Studies:
Das Salk Institute for Biological Studies ist eine der weltweit herausragenden Grundlagenforschungseinrichtungen, in der international renommierte Dozenten in einem einzigartigen, kollaborativen und kreativen Umfeld grundlegende Fragen der Biowissenschaften untersuchen. Salk-Wissenschaftler konzentrieren sich sowohl auf die Entdeckung als auch auf die Betreuung zukünftiger Forschergenerationen und leisten bahnbrechende Beiträge zu unserem Verständnis von Krebs, Alterung, Alzheimer, Diabetes und Herz-Kreislauf-Erkrankungen, indem sie Neurowissenschaften, Genetik, Zell- und Pflanzenbiologie und verwandte Disziplinen studieren.
Die Leistungen der Fakultät wurden mit zahlreichen Ehrungen gewürdigt, darunter Nobelpreise und Mitgliedschaften in der National Academy of Sciences. Das 1960 vom Polioimpfpionier Jonas Salk, MD, gegründete Institut ist eine unabhängige gemeinnützige Organisation und ein architektonisches Wahrzeichen.
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu