
December 13, 2019
Erkenntnisse von Salk-Forschern helfen zu erklären, wie manche Krebsarten einer Chemotherapie widerstehen
Erkenntnisse von Salk-Forschern helfen zu erklären, wie manche Krebsarten einer Chemotherapie widerstehen
LA JOLLA – Mitochondrien, winzige Strukturen, die in den meisten Zellen vorkommen, sind für ihre Energieerzeugungsmaschinerie bekannt. Jetzt haben Salk-Forscher eine neue Funktion der Mitochondrien entdeckt: Sie lösen molekulare Alarme aus, wenn Zellen Stress oder Chemikalien ausgesetzt sind, die die DNA schädigen können, wie etwa eine Chemotherapie. Die Ergebnisse, online veröffentlicht in Naturstoffwechsel am 9. Dezember 2019 könnte zu neuen Krebsbehandlungen führen, die verhindern, dass Tumore gegen Chemotherapie resistent werden.
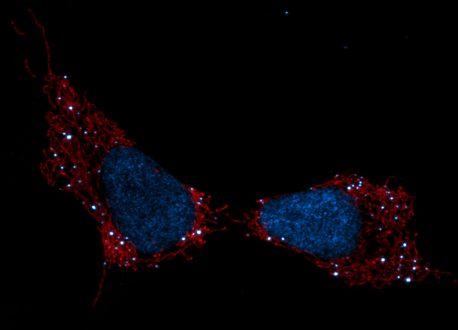
Zu den offenen Stellen für ein hochauflösendes Bild.
Bildnachweis: Salk Institute/Waitt Advanced Biophotonics Center
„Mitochondrien fungieren als erste Verteidigungslinie bei der Erkennung von DNA-Stress. Die Mitochondrien sagen dem Rest der Zelle: ‚Hey, ich werde angegriffen, du solltest dich besser schützen‘“, sagt er Gerald Shadel, Professor am Salk Molecular and Cell Biology Laboratory und am Audrey Geisel Chair in Biomedical Science.
Der Großteil der DNA, die eine Zelle zum Funktionieren benötigt, befindet sich im Zellkern, ist in Chromosomen verpackt und wird von beiden Elternteilen geerbt. Aber Mitochondrien enthalten jeweils ihre eigenen kleinen DNA-Kreise (mitochondriale DNA oder mtDNA genannt), die nur von einer Mutter an ihre Nachkommen weitergegeben werden. Und die meisten Zellen enthalten Hunderte – oder sogar Tausende – Mitochondrien.
Shadels Laborgruppe zuvor gezeigt dass Zellen auf falsch verpackte mtDNA ähnlich reagieren, wie sie auf ein eindringendes Virus reagieren würden – indem sie es aus den Mitochondrien freisetzen und eine Immunantwort auslösen, die die Abwehrkräfte der Zelle stärkt.
In der neuen Studie wollten Shadel und seine Kollegen genauer untersuchen, welche molekularen Wege durch die Freisetzung beschädigter mtDNA in das Zellinnere aktiviert werden. Sie konzentrierten sich auf eine Untergruppe von Genen, die als Interferon-stimulierte Gene (ISGs) bekannt sind und typischerweise durch die Anwesenheit von Viren aktiviert werden. Aber in diesem Fall, so stellte das Team fest, handelte es sich bei den Genen um eine bestimmte Untergruppe von ISGs, die durch Viren aktiviert wurden. Und dieselbe Untergruppe von ISGs wird häufig in Krebszellen aktiviert, die eine Resistenz gegen eine Chemotherapie mit DNA-schädigenden Wirkstoffen wie Doxorubicin entwickelt haben.

Zu den offenen Stellen für ein hochauflösendes Bild.
Bildnachweis: Salk Institute
Um Krebs zu zerstören, greift Doxorubicin die Kern-DNA an. Die neue Studie ergab jedoch, dass das Medikament auch die Schädigung und Freisetzung von mtDNA verursacht, was wiederum ISGs aktiviert. Diese Untergruppe von ISGs, so stellte die Gruppe fest, trägt dazu bei, die Kern-DNA vor Schäden zu schützen – und führt so zu einer erhöhten Resistenz gegen das Chemotherapeutikum. Als Shadel und seine Kollegen mitochondrialen Stress in Melanomkrebszellen induzierten, wurden die Zellen resistenter gegen Doxorubicin, wenn sie in Kulturschalen und sogar in Mäusen gezüchtet wurden, da höhere Mengen an ISGs die DNA der Zelle schützten.
„Vielleicht macht die Tatsache, dass mitochondriale DNA in so vielen Kopien in jeder Zelle vorhanden ist und über weniger eigene DNA-Reparaturwege verfügt, sie zu einem sehr wirksamen Sensor für DNA-Stress“, sagt Shadel.
In den meisten Fällen, betont er, ist es wahrscheinlich gut, dass die mtDNA anfälliger für Schäden ist – sie verhält sich wie ein Kanarienvogel in einer Kohlenmine, um gesunde Zellen zu schützen. Bei Krebszellen bedeutet dies jedoch, dass Doxorubicin – indem es zuerst die mtDNA schädigt und die molekularen Alarmglocken auslöst – bei der Schädigung der Kern-DNA von Krebszellen weniger wirksam sein kann.
„Für mich heißt es, dass man diese Form der Chemotherapie-Resistenz verhindern könnte, wenn man eine Schädigung der mitochondrialen DNA oder deren Freisetzung während der Krebsbehandlung verhindern kann“, sagt Shadel.
Seine Gruppe plant zukünftige Studien darüber, wie genau mtDNA beschädigt und freigesetzt wird und welche DNA-Reparaturwege von den ISGs im Zellkern aktiviert werden, um Schäden abzuwehren.
Weitere Autoren der Studie waren Zheng Wu, Kailash Mangalhara, Alva Sainz, Laura Newman, Victoria Tripple und Susan Kaech von Salk; Sebastian Oeck, Lizhen Wu, Qin Yan, Marcus Bosenberg, Yanfeng Liu, Parker Sulkowski und Peter Glazer von der Yale School of Medicine; Phillip West vom Texas A&M College of Medicine; und Xiao-Ou Zhang von der University of Massachusetts Medical School.
Die Arbeit und die beteiligten Forscher wurden durch Zuschüsse der National Institutes of Health, des Cancer Prevention and Research Institute of Texas, des Office of the Assistant Secretary of Defense for Health Affairs, des China Scholarship Counsel, des Salk Excellerators Postdoctoral Fellowship und unterstützt das Postdoktorandenstipendium der George E. Hewitt Foundation for Medical Research.
DOI: 10.1038/s42255-019-0150-8
JOURNAL
Naturstoffwechsel
AUTOREN
Zheng Wu, Sebastian Oeck, A. Phillip West, Kailash C. Mangalhara, Alva G. Sainz, Laura E. Newman, Xiao-Ou Zhang, Lizhen Wu, Qin Yan, Marcus Bosenberg, Yanfeng Liu, Parker L. Sulkowski, Victoria Tripple , Susan M. Kaech, Peter M. Glazer und Gerald S. Shadel
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu
Das Salk Institute ist ein unabhängiges, gemeinnütziges Forschungsinstitut, das 1960 von Jonas Salk, dem Entwickler des ersten sicheren und wirksamen Polio-Impfstoffs, gegründet wurde. Das Institut hat es sich zur Aufgabe gemacht, grundlegende, kooperative und risikoreiche Forschung zu betreiben, die sich mit den drängendsten gesellschaftlichen Herausforderungen wie Krebs, Alzheimer und der Anfälligkeit der Landwirtschaft auseinandersetzt. Diese Grundlagenforschung bildet die Basis für alle translationalen Bemühungen und generiert Erkenntnisse, die weltweit die Entwicklung neuer Medikamente und Innovationen ermöglichen.