
10 de Junio de 2010
LA JOLLA, CA—Los poros nucleares son los principales guardianes que median la comunicación entre el núcleo de una célula y su citoplasma. Recientemente, también se ha demostrado que estos grandes canales de transporte multiproteico desempeñan un papel esencial en la regulación génica del desarrollo. Sin embargo, a pesar del papel crítico en la función nuclear, los complejos de poros nucleares siguen siendo figuras un tanto sombrías, con muchos detalles sobre su formación envueltos en misterio.
Ahora, un equipo de investigadores del Instituto Salk de Estudios Biológicos ha iluminado las diferencias clave en los mecanismos detrás de los poros nucleares formados en dos etapas distintas del ciclo celular. Sus hallazgos, que se publicarán en la edición del 12 de junio de Cell, pueden brindar información sobre afecciones como el cáncer, los defectos del desarrollo y el paro cardíaco repentino.
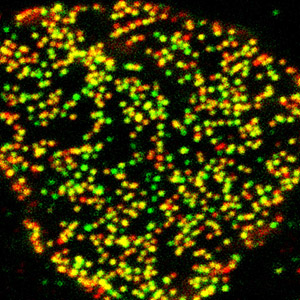
Los poros nucleares, los canales más importantes que controlan el flujo de información dentro y fuera del núcleo de una célula, se ensamblan durante la interfase y después de la mitosis, cuando la membrana nuclear se reforma alrededor de los cromosomas segregados para crear dos núcleos idénticos. La imagen de arriba muestra poros nucleares completamente ensamblados en rojo e intermedios de poros nucleares tempranos en verde.
Imagen: Cortesía de la Dra. Jessica Talamas, Instituto Salk de Estudios Biológicos.
Los poros nucleares, que se construyen a partir de 30 proteínas diferentes, se ensamblan durante la interfase, el período en que el núcleo se expande y replica su ADN, y después de la mitosis, cuando la membrana nuclear se reforma alrededor de los cromosomas segregados para crear dos núcleos idénticos.
Pero, explica Martín Hetzer, Ph.D., profesor asociado de Hearst Endowment en el Laboratorio de Biología Molecular y Celular de Salk, quien dirigió el estudio, ha habido una pregunta de larga data sobre si las vías de ensamblaje en las distintas etapas del ciclo celular usan mecanismos diferentes o similares. “El ensamblaje de la interfase es diferente del ensamblaje posmitótico en que la membrana nuclear se forma completamente alrededor de la cromatina”, dice, “mientras que el ensamblaje posmitótico ocurre en la membrana nuclear en reformación. Entonces, la topología de la membrana nuclear es muy diferente durante estas dos etapas del ciclo celular”.
Si bien se conocían algunos aspectos del ensamblaje posmitótico, casi nada se entendía acerca de cómo se produce el ensamblaje de los poros durante la interfase, cuando la célula duplica el número de poros nucleares para proporcionar niveles suficientes de componentes NPC para las dos células hijas. Un proceso paralelo tiene lugar durante la diferenciación de un ovocito, cuando millones de componentes del poro nuclear se integran en la membrana nuclear del óvulo, por lo que cualquier hallazgo sobre el ensamblaje de la interfase también podría ser relevante para el desarrollo embrionario.
"Pudimos mostrar por primera vez que hay dos mecanismos distintos detrás de cómo estos grandes complejos de proteínas se ensamblan para adaptarse a las diferencias dependientes del ciclo celular en la topología de la membrana nuclear", dice Hetzer.
El equipo identificó una diferencia clave en cómo el complejo Nup107/160, que es esencial para la formación de NPC, está dirigido a nuevos sitios de reunión en el NE. Sorprendentemente, uno de los miembros del complejo, Nup133, se dirige al sitio de ensamblaje de los poros a través de un mecanismo completamente nuevo que implica la detección de la curvatura de la membrana nuclear. "El sensor se identificó en una pantalla de bioinformática y no se sabía si era realmente funcional in vivo", dice la coautora Christine Doucet, Ph.D., becaria postdoctoral en el laboratorio de Hetzer. “Pero pensamos que encajaría con la topología de la membrana nuclear y los sitios de los nuevos complejos de poros nucleares porque están muy curvados. Entonces, si el sensor estaba desempeñando un papel en el ensamblaje, era una forma realmente ingeniosa de coordinar el ensamblaje de todos los componentes en la posición correcta y en el momento correcto”.
La segunda diferencia que descubrió el grupo es que en el ensamblaje posmitótico, pero no durante la interfase, una proteína llamada ELYS desempeñó un papel clave en la dirección del complejo NUP107/160, que es fundamental para la formación de poros, a los sitios de ensamblaje. Por el contrario, la transmembrana Nup POM121 se requiere específicamente para el ensamblaje de interfase. POM121 es la proteína más antigua conocida en los sitios de ensamblaje de poros, pero aún se está investigando cómo se dirige allí.
"Sabíamos que ambas proteínas eran esenciales para el ensamblaje de los poros de diferentes maneras, pero no sabíamos cómo", dice la coautora principal Jessica Talamas, también becaria postdoctoral en el laboratorio de Hetzer. “Hubo una discrepancia en la literatura sobre POM121, por lo que estábamos tratando de averiguar qué estaba pasando. Fue uno de esos momentos de iluminación, estábamos mirando los datos y nos dimos cuenta de que POM121 solo se requería para el ensamblaje de la interfase, y luego todo tuvo sentido”.
Debido a que estos procesos están en funcionamiento en cada célula que se divide, el estudio es especialmente relevante para una de las grandes preguntas en el campo: cómo se regula la cantidad de poros nucleares. Es una pregunta con múltiples ramificaciones. El número de poros nucleares está mal regulado en las células cancerosas, por ejemplo, por lo que los hallazgos tienen aplicaciones en la investigación del cáncer. Además, debido a que las neuronas requieren una gran cantidad de poros nucleares, cada vez hay más pruebas de que los defectos en el ensamblaje de los poros nucleares están relacionados con defectos de desarrollo en el sistema nervioso central. Los defectos de ensamblaje durante el desarrollo también se han implicado en condiciones como el paro cardíaco repentino.
“Al establecer las diferencias entre las dos vías de ensamblaje, los hallazgos han brindado el primer vistazo de una comprensión mecanicista”, dice Hetzer.
Este estudio fue apoyado por una subvención de los Institutos Nacionales de Salud.
Acerca del Instituto Salk de Estudios Biológicos
El Instituto Salk de Estudios Biológicos es una de las instituciones de investigación básica más importantes del mundo, donde profesores de renombre internacional investigan cuestiones fundamentales de las ciencias de la vida en un entorno único, colaborativo y creativo. Centrados tanto en el descubrimiento como en la orientación de futuras generaciones de investigadores, los científicos de Salk realizan contribuciones innovadoras a nuestra comprensión del cáncer, el envejecimiento, el Alzheimer, la diabetes y los trastornos cardiovasculares mediante el estudio de la neurociencia, la genética, la biología celular y vegetal y disciplinas relacionadas.
Los logros de la facultad han sido reconocidos con numerosos honores, incluidos premios Nobel y membresías en la Academia Nacional de Ciencias. Fundado en 1960 por el pionero de la vacuna contra la polio Jonas Salk, MD, el Instituto es una organización independiente sin fines de lucro y un hito arquitectónico.
Oficina de Comunicaciones
Tel: (858) 453-4100
prensa@salk.edu