
23 Maggio 2013
Le sorprendenti scoperte dei ricercatori del Salk offrono la speranza che la terapia attualmente in fase di sperimentazione sul cancro avanzato possa arrestare la progressione delle cellule premaligne
Le sorprendenti scoperte dei ricercatori del Salk offrono la speranza che la terapia attualmente in fase di sperimentazione sul cancro avanzato possa arrestare la progressione delle cellule premaligne
LA JOLLA, CA—Gli scienziati hanno scoperto un meccanismo di sopravvivenza che si verifica nelle cellule del seno appena trasformate in cellule premaligne, ovvero a metà strada tra la normalità e il cancro, e che potrebbe portare a nuovi metodi per fermare i tumori.
Nel loro Cellula molecolare uno studio, i ricercatori del Salk Institute riferiscono che una proteina nota come fattore di crescita trasformante beta (TGF-β), considerata un soppressore del tumore nello sviluppo precoce del cancro, può in realtà promuovere cancro una volta che una cellula entra in uno stato precanceroso.
La scoperta, una sorpresa per i ricercatori, solleva l'allettante possibilità che, con un nuovo trattamento, alcuni tumori possano essere prevenuti prima ancora che si sviluppino.

Fernando Lopez-Diaz e Beverly M. Emerson del Regulatory Biology Laboratory presso Salk.
Immagini: per gentile concessione del Salk Institute for Biological Studies
"Il nostro lavoro suggerisce che potrebbe essere possibile arrestare lo sviluppo del cancro nelle cellule premaligne, quelle che sono a poche divisioni dall'essere normali", afferma l'autore principale dello studio, Fernando Lopez-Diaz, un ricercatore presso Laboratorio di biologia regolatoria a Salk.
Gli agenti progettati per inibire il TGF-β sono già in fase di sperimentazione contro i tumori che si sono già diffusi, afferma Beverly M. Emerson, professoressa del Salk College, responsabile del laboratorio e autrice principale dello studio. "Questo studio offre sia spunti significativi sullo sviluppo precoce del cancro, sia una nuova direzione da esplorare nel trattamento del cancro", afferma. "Sarebbe fantastico se un singolo agente potesse bloccare sia il cancro avanzato che quello pronto a svilupparsi".
Gli oncologi potrebbero anche essere in grado di utilizzare la loro scoperta per prevedere se le cellule premaligne di un paziente siano destinate a trasformarsi in un tumore a tutti gli effetti, aggiunge Emerson. "Non tutte le cellule premaligne si trasformano in tumore", afferma. "Molte si autodistruggono a causa di meccanismi di protezione cellulare. Ma alcune diventeranno tumori e, a questo punto, non c'è modo di prevedere quali di queste cellule siano a rischio".
Le molecole di TGF-β sono proteine secrete presenti nella maggior parte dei tessuti umani. Svolgono diversi ruoli biologici, tra cui il controllo della proliferazione cellulare e dell'infiammazione e il supporto alla guarigione delle ferite.
Il dogma prevalente nella ricerca sul cancro è che la segnalazione del TGF-β impedisca alle cellule di trasformarsi in cancro, afferma Lopez-Diaz. Gli scienziati hanno anche riconosciuto che le cellule tumorali che "vogliono" diffondersi imparano a usare la funzione di guarigione delle ferite del TGF-β per staccarsi dal tumore, afferma.
Un'altra proteina, la P53, è un noto soppressore tumorale. Durante la risposta allo stress che si verifica quando una cellula diventa cancerosa, e in risposta alla chemioterapia, la p53 tenta di riparare il danno al DNA che si è verificato e, se non ci riesce, ordina alla cellula di morire. "Il percorso della p53 deve essere sabotato affinché le cellule diventino cancerose", afferma Lopez-Diaz. "Questo accade quando il suo gene subisce una mutazione, se la proteina p53 viene degradata eccessivamente o, cosa meno nota, se la biosintesi della p53 viene impedita".
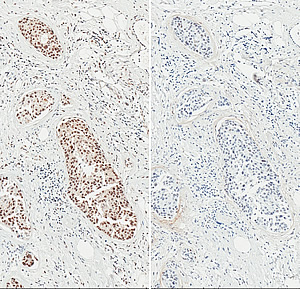
Questa immagine mostra in marrone l'attivazione della segnalazione TGFβ (a sinistra) e i livelli di p53 (a destra) in una biopsia mammaria di una paziente a cui è stato diagnosticato un carcinoma duttale in situ e un carcinoma invasivo. Il TGFβ1 disattiva il pathway principale che dirige la risposta ai farmaci chemioterapici e allo stress cellulare, suggerendo una potenziale nuova terapia per prevenire la progressione dei tumori in fase iniziale e la resistenza ai farmaci.
Immagini: per gentile concessione del Salk Institute for Biological Studies
I ricercatori hanno condotto questo studio per comprendere esattamente come p53 e TGF-β interagiscono nello sviluppo del cancro. "Nell'ultimo decennio, tutti hanno creduto che questi due percorsi lavorassero insieme nelle cellule normali e premaligne per fermare il cancro, anche se non c'erano molti dati a supporto di questa ipotesi", afferma.
Il team ha esaminato cellule premaligne e cancerose provenienti da tumori al seno e ai polmoni e ha confrontato cellule mammarie normali e premaligne di donne sane fornite dagli scienziati dell'Università della California di San Francisco.
Ma indipendentemente dal modo in cui hanno condotto i loro esperimenti, i ricercatori del Salk hanno scoperto che il TGF-β può interferire con le risposte delle cellule ai danni nelle cellule premaligne o cancerose.
Hanno infatti scoperto che il TGF-β blocca sia la trascrizione del gene p53, il processo mediante il quale i meccanismi cellulari leggono il codice del DNA per un gene, sia il successivo processo mediante il quale viene prodotta la proteina p53 corrispondente, noto come traduzione.
Questo potrebbe spiegare perché, in circa la metà dei tumori al seno, comprese le lesioni premaligne, studiati dal team sia presso l'UC San Francisco che presso il Sanford Burnham Medical Research Institute, quando la segnalazione del TGF-β1 era altamente attivata, i livelli di p53 si riducevano e viceversa: se la via del TGF-β1 era ridotta, si riscontravano alti livelli di p53. "Una tendenza simile è stata osservata con PUMA, una proteina che induce la morte cellulare", aggiunge Fernando Lopez-Diaz. "C'era una proteina PUMA piuttosto abbondante quando l'attivazione del TGF-β1 era scarsa e viceversa."
"Il lato negativo del TGF-β è emerso a poche divisioni cellulari dalla normalità, consentendo alle cellule di evitare la morte", afferma.
Questa ritrovata immortalità spiega molti misteri oncologici, afferma Lopez-Diaz. "Uno di questi è che getta luce su come le cellule tumorali precancerose e in fase iniziale siano in grado di resistere all'assalto della chemioterapia e di altri trattamenti", afferma.
Potrebbe spiegare perché il 77 percento dei tumori al seno presenta un gene p53 normale e suggerisce inoltre un modo in cui le cellule tumorali possono utilizzare entrambi per metastatizzare e sopravvivere al viaggio verso gli organi in cui stabiliscono una nuova casa.
"Poiché aiuta le cellule a evitare la morte, il TGF-β può ridurre l'impatto negativo che il processo metastatico ha sulle cellule cancerose", afferma Lopez-Diaz.
Aggiunge che c'è ancora molto lavoro da fare. "Vogliamo comprendere i segnali che trasformano il TGF-β in un nemico", afferma. "Se lo scoprissimo, potremmo essere in grado di inibire quei segnali e indurre le cellule danneggiate a morire, come dovrebbero. Questo potrebbe offrirci un'altra possibilità terapeutica, insieme agli inibitori del TGF-β attualmente in fase di sperimentazione".
Altri autori dello studio sono Sri Kripa Balakrishnan, del Salk; Philippe Gascard, Jianxin Zhao e Thea D. Tlsty, dell'Università della California di San Francisco; e Sonia V. del Rincon e Charles Spruck, del Sanford Burnham Medical Research Institute.
Lo studio è stato finanziato da sovvenzioni del National Cancer Institute (U54CA143803), la Chambers Medical Foundation
e una borsa di studio del Cancer Center (P30 CA014195).
Informazioni sul Salk Institute for Biological Studies:
Il Salk Institute for Biological Studies è uno dei più importanti istituti di ricerca di base al mondo, dove docenti di fama internazionale affrontano questioni fondamentali delle scienze della vita in un ambiente unico, collaborativo e creativo. Concentrati sia sulla scoperta che sulla formazione delle future generazioni di ricercatori, gli scienziati del Salk forniscono contributi innovativi alla nostra comprensione di cancro, invecchiamento, Alzheimer, diabete e malattie infettive, studiando neuroscienze, genetica, biologia cellulare e vegetale e discipline correlate.
I risultati conseguiti dal corpo docente sono stati riconosciuti con numerosi riconoscimenti, tra cui premi Nobel e l'iscrizione alla National Academy of Sciences. Fondato nel 1960 dal pioniere del vaccino contro la poliomielite Jonas Salk, l'Istituto è un'organizzazione indipendente senza scopo di lucro e un punto di riferimento architettonico.
JOURNAL
Cellula molecolare
AUTORI
Fernando J. Lopez-Diaz, Philippe Gascard, Sri kripa Balakrishnan, Jianxin Zhao, Sonia Valle del Rincon, Charles Spruck, Thea D. Tlsty, Beverly M. Emerson
Ufficio delle comunicazioni
Tel: (858) 453-4100
press@salk.edu