
December 13, 2010
LA JOLLA, CA - Een nauwe samenwerking tussen onderzoekers van het Salk Institute for Biological Studies en het Institute for Advanced Study ontdekte dat de tumoronderdrukker p53, lang beschouwd als de "bewaker van het genoom", meer kan doen dan kanker veroorzaken mutaties. Het kan ook voorkomen dat gevestigde kankercellen afglijden naar een meer agressieve, stengelachtige toestand door te dienen als een "hoeder tegen herprogrammering van het genoom".
Het nieuwe werk, gemeld door Geoffrey M.Wahl, Ph.D., en Benjamin Spike, Ph.D., bij Salk Institute en Arnold J. Levine, Ph.D., en Hideaki Mizuno, Ph.D., bij IAS, Princeton, in de online editie van deze week van de Proceedings van de National Academy of Sciences, onthulde opvallende parallellen tussen de verhoogde herprogrammeringsefficiëntie van normale volwassen cellen zonder p53, de inherente plasticiteit en tumorigeniciteit van stamcellen en de hoge incidentie van p53-mutaties bij kwaadaardige kankers.
"Een slecht gedifferentieerd uiterlijk, cellulaire en genetische heterogeniteit zijn bekende kenmerken van veel agressieve en dodelijke kankers", legt Wahl uit, een professor in het Gene Expression Laboratory in Salk, "en er is onlangs gesuggereerd dat deze eigenschappen het gevolg zijn van de aanwezigheid van stamachtige kankercellen. Onze bevindingen geven aan dat p53-mutaties cellen in een tumor in staat zouden kunnen stellen de tijd terug te draaien door een stamcelachtig 'programma' te verwerven.”
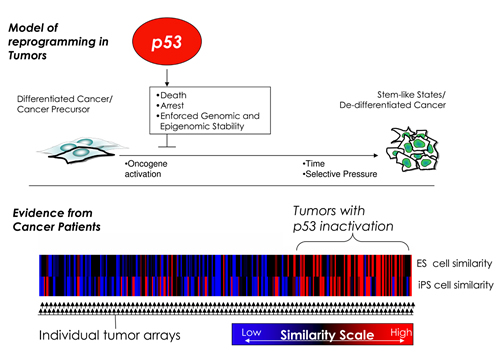
De tumoronderdrukker p53 voorkomt dat gevestigde kankercellen naar een meer agressieve, stengelachtige toestand glijden.
Illustratie: Met dank aan Dr. Benjamin Spike, Salk Institute for Biological Studies.
Kankercellen moeten enkele kenmerken van stamcellen verwerven om te overleven en zich aan te passen aan steeds veranderende omgevingen. Deze omvatten onsterfelijkheid, het vermogen om zichzelf te vernieuwen en het vermogen om voorlopers te produceren die differentiëren in andere celtypen. "Elke tumor vertegenwoordigt een diverse verzameling kankercellen", zegt Wahl, "en de vraag was hoe het beste kan worden verklaard hoe een dergelijke heterogeniteit ontstaat."
In het verleden werd de cellulaire diversiteit van kankers meestal toegeschreven aan genetische instabiliteit, die vele jaren geleden door Wahl en zijn team werd aangetoond wanneer p53 is uitgeschakeld. Naarmate de tumorcelpopulatie zich uitbreidt, zo luidt de heersende theorie, pikken individuele cellen willekeurige mutaties op en begint hun moleculaire identiteit uiteen te lopen. Tegen de tijd dat de kanker wordt ontdekt, zijn de miljoenen cellen waaruit de tumor bestaat zo verschillend van elkaar geworden als neven en nichten die twee keer zijn verwijderd.
Er was ook een lang bestaand idee dat volledig toegewijde en gespecialiseerde cellen zouden kunnen de-differentiëren in de loop van de tumor-initiatie en -progressie, hoewel het onduidelijk was hoe dit zou kunnen worden bereikt. Uiteindelijk werd de theorie verworpen ten gunste van de momenteel modieuze kankerstamceltheorie, die stelt dat kankerstamcellen - de cellen die een tumor voortplanten en die mogelijk kunnen voortkomen uit een normale stam of vroege voorlopercellen - verschillen van het grootste deel van de kankercellen. in die zin dat ze zichzelf kunnen vernieuwen en niet-stamcellen kunnen produceren, net zoals normale stamcellen dat doen.
"Onze bevindingen geven aan dat kankercellen die op stamcellen lijken geen deel hoeven uit te maken van de oorspronkelijke tumor, maar eerder kunnen ontstaan tijdens latere stadia van tumorontwikkeling, mogelijk gemaakt door het verlies van p53", zegt postdoctoraal onderzoeker en co-eerste auteur Benjamin T. Spike , Ph.D. “De waargenomen tumorheterogeniteit is waarschijnlijk een combinatie van groeiende genomische instabiliteit en epigenetische instabiliteit geassocieerd met de verwerving van een stamcelachtig fenotype."
Wahl en zijn team overwogen eerst de mogelijkheid dat p53 meer doet dan functioneren als een "genoombewaker" toen een gezamenlijke studie met Juan-Carlos Izpisúa Belmonte, Ph.D., ook een professor in het Gene Expression Laboratory van het Salk Institute, onthulde dat deze tumoronderdrukker ook een barrière vormt voor de herprogrammering van somatische cellen.
Om erachter te komen of p53-inactivatie het ontstaan van op stamcellen lijkende tumorcellen mogelijk maakt, kamden Spike en Mizuno door honderden archief-genexpressieprofielen van borst- en longtumoren, op zoek naar stamcelachtige handtekeningen en correleerden ze met hun p53-status.
"We vonden een nauwe correlatie tussen tumoren met bevestigde p53-mutaties of openlijke p53-inactivatie en genexpressiepatronen die typerend zijn voor stamcellen", legt Spike uit. "Het zal de manier beïnvloeden waarop we over p53 denken, aangezien het verlies ervan nu een weerkaatsing lijkt te hebben die verder gaat dan het verwijderen van de onmiddellijke celdood en proliferatiebarrières voor tumorigeniciteit."
Wahl hoopt dat het verkrijgen van een beter begrip van het proces dat ervoor zorgt dat tumorcellen terugkeren naar een meer stengelachtige staat, nieuwe doelen voor therapeutische interventie zal onthullen. "Meer stengelachtige tumoren lijken agressiever te zijn, maar ze kunnen nog steeds een restcapaciteit hebben om te differentiëren in minder agressieve celtypen", zegt hij. "Als we dit potentieel kunnen aanboren, kunnen we deze cellen misschien dwingen om te differentiëren om minder gevaarlijk te worden, wat een oud idee is dat we serieus moeten heroverwegen."
De hechtheid van de samenwerking wordt aangegeven door het delen van het eerste auteurschap tussen Spike en Mizuno, die nu werkzaam is bij Chugai Pharmaceutical Co. Ltd., in Kamakura, Japan.
Het werk bij Salk werd gefinancierd door de Breast Cancer Research Foundation, de G. Harold en Leila Y. Mathers Charitable Foundation, het National Cancer Institute en een Ruth L. Kirschstein National Research Service Award.
Over het Salk Instituut voor Biologische Studies
Het Salk Institute for Biological Studies is een van 's werelds meest vooraanstaande instellingen voor fundamenteel onderzoek, waar internationaal gerenommeerde faculteiten fundamentele levenswetenschappelijke vragen onderzoeken in een unieke, collaboratieve en creatieve omgeving. Salk-wetenschappers zijn zowel gericht op ontdekking als op het begeleiden van toekomstige generaties onderzoekers en leveren baanbrekende bijdragen aan ons begrip van kanker, veroudering, Alzheimer, diabetes en infectieziekten door neurowetenschappen, genetica, cel- en plantenbiologie en aanverwante disciplines te bestuderen.
Faculteitsprestaties zijn erkend met tal van onderscheidingen, waaronder Nobelprijzen en lidmaatschappen van de National Academy of Sciences. Het instituut, opgericht in 1960 door poliovaccinpionier Jonas Salk, MD, is een onafhankelijke non-profitorganisatie en architectonisch monument.
Het Salk Institute viert met trots vijf decennia van wetenschappelijke excellentie in fundamenteel onderzoek.
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu