
November 2, 2015
Door meer dan 4,000 genen in menselijke tumoren te testen, ontdekte een Salk-team een enzym dat verantwoordelijk is voor het onderdrukken van een veelvoorkomende en dodelijke longkanker
Door meer dan 4,000 genen in menselijke tumoren te testen, ontdekte een Salk-team een enzym dat verantwoordelijk is voor het onderdrukken van een veelvoorkomende en dodelijke longkanker
LA JOLLA – Wetenschappers van het Salk Institute hebben een molecuul ontdekt waarvan de mutatie leidt tot de agressieve groei van een veelvoorkomend en dodelijk type long kanker bij mensen.
Dit enzym, EphA2 genaamd, regelt normaal gesproken een gen dat verantwoordelijk is voor weefselgroei. Maar wanneer EphA2 is gemuteerd, ontdekte het Salk-team, kunnen cellulaire systemen amok maken en snel tumoren ontwikkelen. Het nieuwe werk verscheen in de week van 2 november 2015 in PNAS, suggereert dat EphA2 een nieuw doelwit zou kunnen zijn voor een subgroep van longkanker, die zowel niet-rokers als rokers treft, en wereldwijd de belangrijkste oorzaak is van aan kanker gerelateerde sterfgevallen.
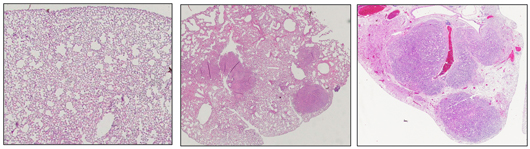
Wetenschappers van Salk ontdekken bij mensen een molecuul genaamd EphA2 dat werkt als een tumoronderdrukker bij bepaalde soorten longkanker. Deze afbeelding toont normaal muizenlongweefsel (links) en longen met tumoren als gevolg van een KRAS-mutatie (midden). Wanneer EphA2 wordt uitgeschakeld, resulteert de KRAS-mutatie in veel meer en grotere tumoren in hetzelfde tijdsbestek (rechts).
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
"Soms zijn er honderden mutaties in de genen van de tumoren van een patiënt, maar je weet niet of ze aanjagers zijn van de ziekte of bijproducten", zegt senior auteur Onder Verma, hoogleraar genetica en houder van Salk's Irwin en Joan Jacobs Chair in Exemplary Life Science. "We hebben een nieuwe manier gevonden om kankeronderdrukkende genen te identificeren en te begrijpen hoe ze kunnen worden gericht op therapieën."
Van twee genmutaties is met name bekend dat ze de groei van menselijke tumoren stimuleren: KRAS en p53. Hoewel beide genen zwaar zijn bestudeerd, zijn ze moeilijk therapeutisch aan te pakken, dus besloot het Salk-team om in plaats daarvan naar genen te kijken die KRAS en p53 zouden kunnen controleren.
De onderzoekers beperkten zich tot de 4,700 genen in het menselijk genoom die verband houden met cellulaire signalering, met name genen die het vermogen hebben om celgroei en -proliferatie te remmen. Vervolgens paste het team een genetische screeningtechniek aan om snel en efficiënt het effect van deze duizenden genen op de ontwikkeling van tumoren te testen. In diermodellen ontdekte het Salk-team dat 16 van deze celsignaleringsgenen moleculen produceerden die een significant effect hadden op KRAS- en p53-gerelateerde tumoren.
Van deze 16 moleculen viel er één vooral op: het EphA2-enzym, oorspronkelijk ontdekt in het laboratorium van een andere Salk-wetenschapper, Tony Jager. Eerder was de betekenis van EphA2 bij longkanker onduidelijk, maar het team ontdekte dat de afwezigheid ervan KRAS-geassocieerde tumoren veel agressiever liet groeien.
“Bij een mutatie in KRAS vormt zich in 300 dagen een tumor. Maar zonder EphA2 leidt de KRAS-mutatie tot tumoren in de helft van de tijd, 120 tot 150 dagen', zegt Verma, die ook hoogleraar Moleculaire Biologie aan de American Cancer Society is. "Dit molecuul EphA2 heeft een enorm effect op het remmen van de groei van kanker wanneer KRAS gemuteerd is." Gemuteerd KRAS is een veelvoorkomende boosdoener bij ongeveer 10 tot 20 procent van alle kankers, met name darmkanker en longkanker bij de mens.

Van links: Salk-onderzoekers Yifeng Xia, Eugene Ke, Narayana Yeddula en Inder Verma
Klik hier voor een afbeelding met hoge resolutie.
Afbeelding: met dank aan het Salk Institute for Biological Studies
"Aangezien het activeren van EphA2 leidde tot de onderdrukking van zowel celsignalering als celproliferatie, denken we dat het enzym zou kunnen dienen als een potentieel medicijndoelwit bij KRAS-afhankelijk longadenocarcinoom", zegt Narayana Yeddula, een onderzoeksmedewerker van Salk en eerste auteur van het artikel. .
Een 10-jarig nationaal project genaamd de Cancer Genome Atlas bracht het genoom van honderden patiënten voor meer dan 20 verschillende vormen van kanker in kaart en bracht een aantal verwante genetische mutaties aan het licht, hoewel de rol van deze mutaties bij longkanker (vooral adenocarcinoom, die goed is voor bijna een kwart van alle longkanker). Uit de gegevens van de Cancer Genome Atlas ontdekte het Salk-team dat genetische veranderingen van EphA2 werden gedetecteerd bij 54 van de 230 patiënten met adenocarcinoom. Het team ontdekte verrassend genoeg ook dat het verlies van EphA2 een pad activeerde dat gewoonlijk wordt geassocieerd met kanker (genaamd Hedgehog) dat tumorgroei bevordert.
“Vreemd genoeg heeft ongeveer 2 procent van de patiënten met menselijke longkanker met EphA8-mutaties een hoge EphA2-expressie. Dus in sommige gevallen onderdrukt EphA2 geen tumoren en kan het contextafhankelijk zijn. Daarom moeten we de functie van het molecuul zorgvuldig evalueren bij het ontwerpen van nieuwe therapieën”, voegt Yifeng Xia toe, een onderzoeker van het Salk-personeel die bij het werk betrokken is.
Andere auteurs op het papier waren Eugene Ke van het Salk Instituut en Joep Beumer van het Salk Instituut en het Hubrecht Instituut in Nederland.
Dit werk werd gedeeltelijk ondersteund door een NIH beurs, een Salk Cancer Center Core-beurs, Ipsen HN en Frances C. Berger Foundationen Leona M. en Harry B. Helmsley Charitable Trust.
BLOG
PNAS
TITEL
Screening op tumoronderdrukkers: verlies van ephrine-receptor A2 werkt samen met oncogene KRAS bij het bevorderen van longadenocarcinoom
AUTEURS
Narayana Yeddula, Yifeng Xia, Eugene Ke, Joep Beumer en Inder M. Verma
Bureau voor communicatie
Tel: (858) 453-4100
pers@salk.edu
Het Salk Institute is een onafhankelijk, non-profit onderzoeksinstituut, opgericht in 1960 door Jonas Salk, de ontwikkelaar van het eerste veilige en effectieve poliovaccin. De missie van het instituut is het stimuleren van fundamenteel, collaboratief en risicovol onderzoek dat de meest urgente maatschappelijke uitdagingen aanpakt, waaronder kanker, de ziekte van Alzheimer en de kwetsbaarheid van de landbouw. Deze fundamentele wetenschap vormt de basis van alle translationele inspanningen en genereert inzichten die wereldwijd nieuwe geneesmiddelen en innovaties mogelijk maken.