Vice-president, Chief Science Officer
Hoogleraar
Laboratorium voor moleculaire en celbiologie
Donald en Darlene Shiley-stoel

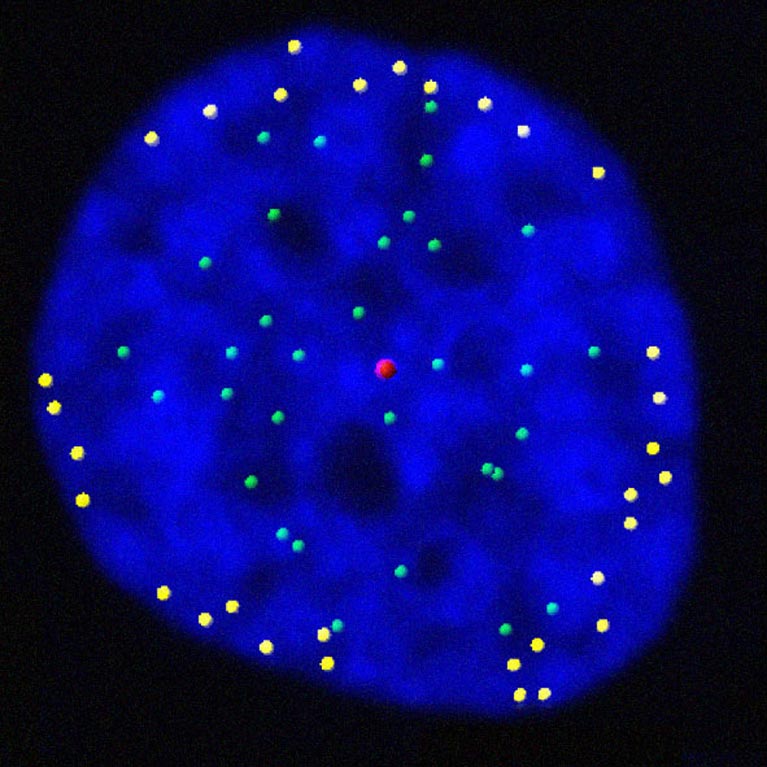
Net zoals elke fotokopie van een kopie iets minder scherp wordt dan de vorige versie, verliest elke keer dat een cel zijn genetisch materiaal kopieert, enkele details van de uiteinden van elk chromosoom. Deze uiteinden, telomeren genaamd, eroderen uiteindelijk en stellen vitale genen bloot aan slijtage, waardoor een cel niet kan groeien of afsterven. Telomeren reguleren belangrijke proliferatieve grenzen en beperken het celgroeipotentieel, en als gevolg daarvan remmen ze de vorming van kanker.
In veel kankercellen worden telomeren echter voortdurend herbouwd, waardoor een cel onsterfelijk wordt. Evenzo neemt het vermogen van de cel om gebroken DNA te repareren af met de leeftijd, wat leidt tot de accumulatie van mutaties en leeftijdsgerelateerde ziekten. Als wetenschappers kunnen bepalen hoe ze deze telomeeruitbreiding kunnen stoppen en het DNA-herstel tijdens veroudering kunnen verbeteren, kunnen ze mogelijk kankercellen laten afsterven of vatbaarder maken voor medicijnen. Aan de andere kant kan het intact houden van telomeren en het verbeteren van DNA-herstel vroegtijdige verouderingssyndromen behandelen. Maar eerst moeten onderzoekers de complexe ins en outs van de normale telomeerfunctie en de regulatie van DNA-reparatie begrijpen.
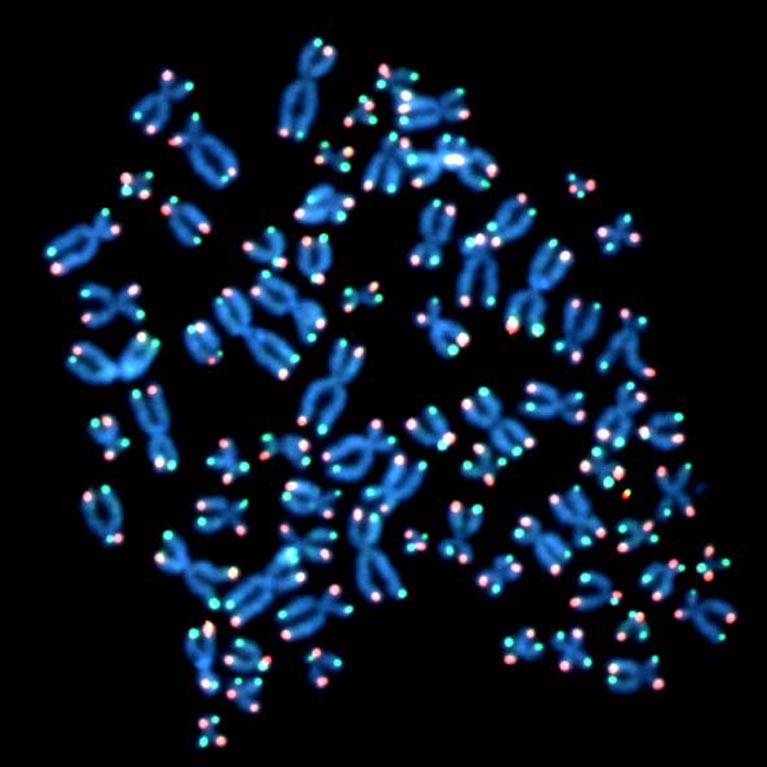
Jan Karlseder bestudeert de rol van telomeren gedurende de proliferatiecyclus van een cel - vanaf het moment dat de cel zijn genetisch materiaal begint te kopiëren tot het moment dat deze zich in twee nieuwe cellen deelt, en gedurende het hele leven van de cel - vanaf het moment dat een jonge cel tevoorschijn komt door celdeling tot wanneer een oude cel permanent "met pensioen gaat" (senescent wordt) of sterft.
Celdelingslimieten, zoals die worden gesteld door telomeerverkorting, zijn essentieel om ongecontroleerde celdeling te beperken en daarmee kankervorming te voorkomen. De twee fundamentele limieten die voorkomen dat primaire menselijke cellen kanker worden, zijn: replicatieve senescentie, een soort cellulaire pensionering waarin cellen stoppen met delen, en crisis, een toestand die leidt tot celdood. Hoewel deze grenzen al tientallen jaren werden erkend, bleef het onduidelijk hoe cellen verouderen en wat er gebeurt als cellen zich blijven delen wanneer ze verouderen.
Door de mechanismen te ontdekken en duidelijk te definiëren die de celdeling van primaire menselijke cellen reguleren (cellen uit levend weefsel zoals een biopsie), heeft het Karlseder-lab nieuwe wegen blootgelegd tijdens de vroegste stadia van kankervorming, die mogelijke interventies kunnen opleveren.
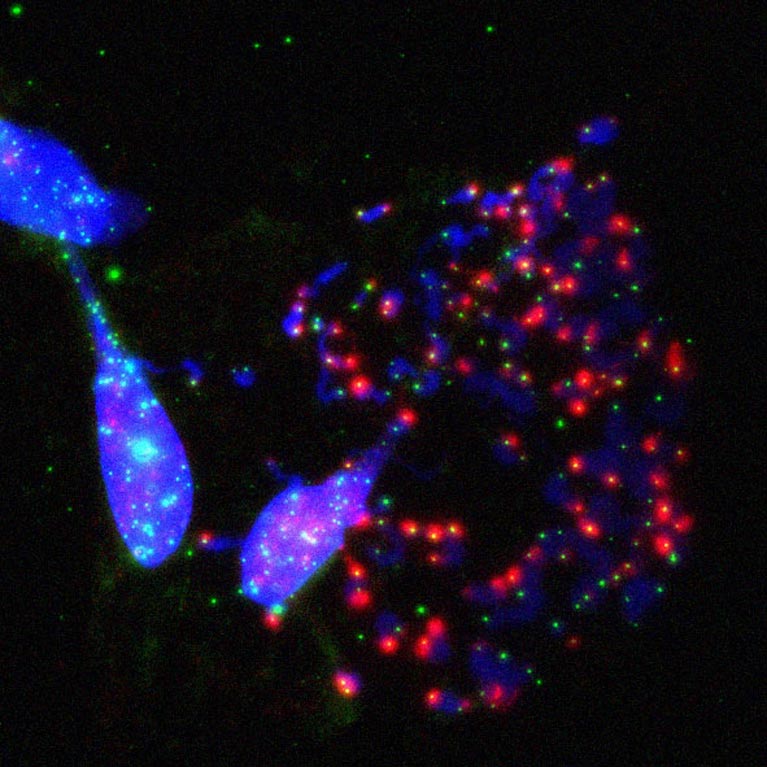
Het Karlseder-lab ontdekte dat celdood in crisis wordt uitgevoerd door de macroautofagie-machinerie, een cellulair recyclingmechanisme, dat een nieuwe tumoronderdrukkende route onthult.
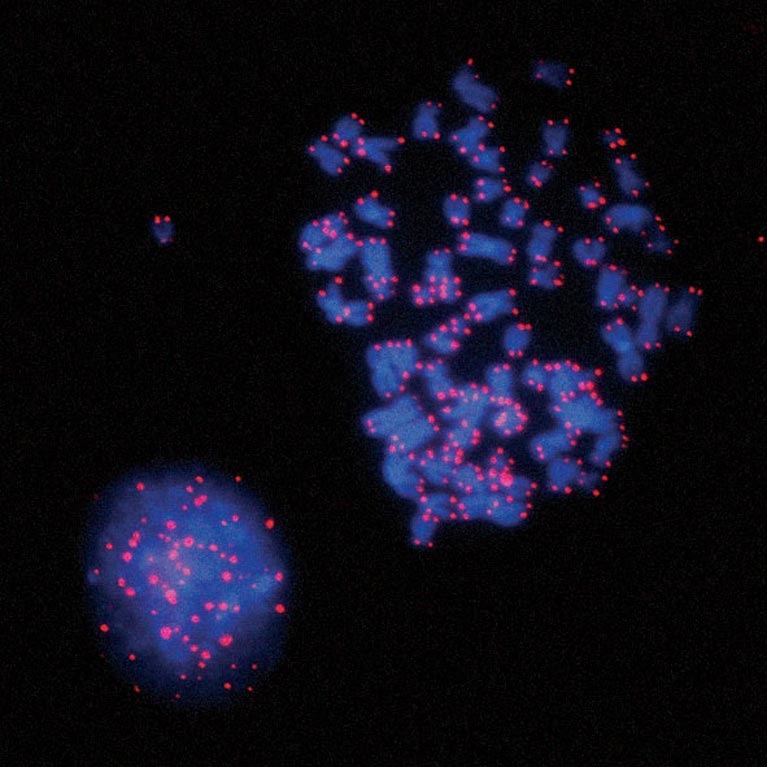
Bij senescentie-bypass worden telomeren verder verkort, totdat de chromosomen samensmelten. Karlseder en zijn team ontdekten dat deze gefuseerde telomeren een cellulair controlepunt (spindelconstructie) activeren dat ervoor zorgt dat de mitotische celdeling stopt, waarbij het schadesignaal wordt versterkt en celdood in een enkele celcyclus veroorzaakt.
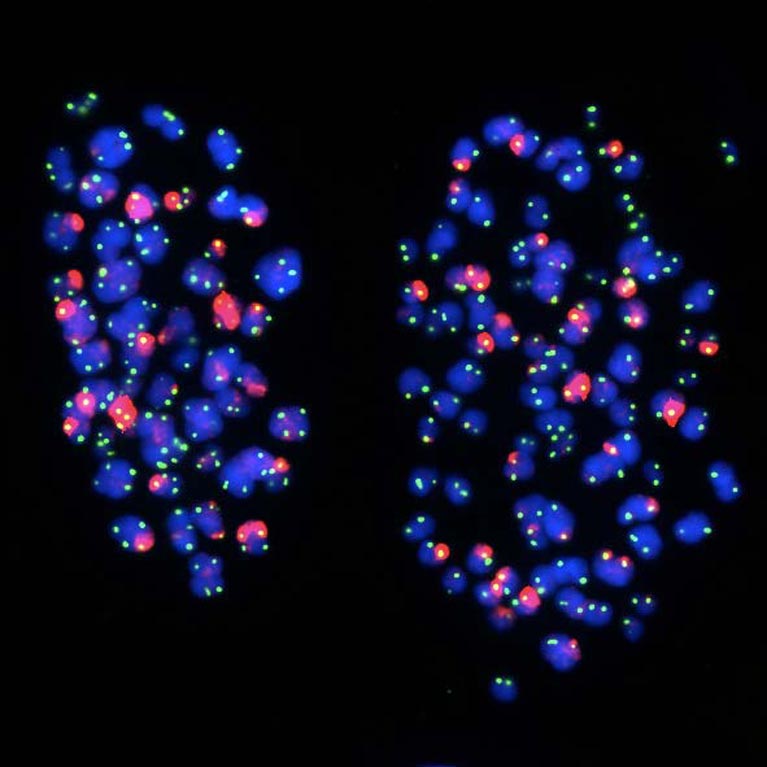
Zijn lab ontdekte dat telomeren na duplicatie naar de buitenrand van de celkern gaan. De bevindingen laten zien hoe onze genen worden gereguleerd en hoe genexpressieprogramma's worden gewijzigd tijdens celdeling, een belangrijke stap in het begrijpen van veroudering en ziekten die voortkomen uit genetische mutaties, zoals kanker.
BS, Biologie, Universiteit van Innsbruck, Oostenrijk
PhD, Moleculaire Biologie, Universiteit van Wenen
Postdoctorale beurs, The Rockefeller University, NY