
17 août 2016
Les scientifiques de Salk révèlent pourquoi les personnes porteuses du gène ApoE4 sont plus sensibles à la maladie d'Alzheimer
Les scientifiques de Salk révèlent pourquoi les personnes porteuses du gène ApoE4 sont plus sensibles à la maladie d'Alzheimer
LA JOLLA — Depuis des décennies, les scientifiques savent que les personnes possédant deux copies d'un gène appelé apolipoprotéine E4 (ApoE4) sont beaucoup plus susceptibles d'avoir La maladie d'Alzheimer À 65 ans, les chercheurs du Salk Institute ont identifié un nouveau lien entre l'ApoE4 et l'accumulation de protéines associée à la maladie d'Alzheimer, ce qui pourrait expliquer biochimiquement comment un excès d'ApoE4 provoque la maladie.
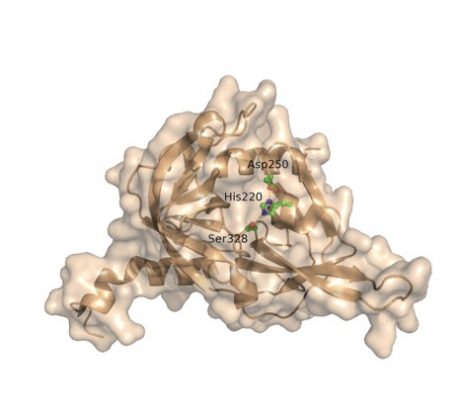
Cliquez ici pour une image haute résolution.
Crédit : Salk Institute
« L’idée générale ici est que nous avons trouvé une façon très différente de penser à la façon dont les protéines dans la maladie d’Alzheimer pourraient être régulées », explique Alan SaghatelianProfesseur Salk et titulaire de la chaire Dr Frederik Paulsen aux Laboratoires de biologie des peptides de la Fondation Clayton de Salk. Leurs conclusions, publiées dans le numéro d'août 2016 de la revue Journal de l'American Chemical Society, soulignent l’importance d’examiner les gènes et les protéines qui ne sont pas classiquement associés à la maladie d’Alzheimer pour progresser dans la compréhension de la maladie.
La maladie d'Alzheimer à début tardif – une forme de la maladie qui touche les personnes de 65 ans et plus – touche plus de 5 millions d'Américains et se caractérise par une perte progressive de la mémoire et une démence. Les scientifiques ont émis diverses hypothèses quant à ses causes, notamment l'accumulation de plaques bêta-amyloïdes et d'enchevêtrements de protéines tau dans le cerveau.
L'apolipoprotéine E existe en trois versions, ou variantes, appelées ApoE2, ApoE3 et ApoE4. Toutes les protéines ApoE ont la même fonction normale : transporter les lipides, le cholestérol et les vitamines dans tout l'organisme, y compris vers le cerveau. Si l'ApoE2 a un effet protecteur et que l'ApoE3 semble n'avoir aucun effet, une mutation de l'ApoE4 est un facteur de risque génétique bien établi pour la maladie d'Alzheimer à début tardif. Des études antérieures ont suggéré qu'ApoE4 pourrait affecter la façon dont le cerveau élimine la bêta-amyloïde, mais ce qui se passe au niveau moléculaire n'est pas clair.
« L'ApoE4 est la mutation génétique la plus prédictive de la maladie d'Alzheimer à début tardif, mais personne n'a vraiment compris ce qui se passe au niveau moléculaire », explique Saghatelian. Les scientifiques avaient cependant déjà découvert des indices indiquant que l'ApoE4 pourrait se dégrader différemment des autres variants, mais la protéine responsable de cette dégradation demeurait inconnue.
Pour trouver la protéine responsable de la dégradation de l'ApoE4, Saghatelian et son associé de recherche Qian Chu, premier auteur du nouvel article, ont examiné les tissus à la recherche de suspects potentiels et se sont concentrés sur une enzyme appelée sérine peptidase A1 à haute température (HtrA1).
En comparant la façon dont HtrA1 dégradait l'ApoE4 avec l'ApoE3, ils ont constaté que l'enzyme transformait davantage l'ApoE4 que l'ApoE3, la décomposant en fragments plus petits et moins stables. Les chercheurs ont confirmé cette observation à la fois sur des protéines isolées et sur des cellules humaines. Cette découverte suggère que les cellules cérébrales des personnes porteuses d'ApoE4 pourraient contenir moins d'ApoE, et davantage de produits de dégradation de la protéine.

Cliquez ici pour une image haute résolution
Crédit : Salk Institute
« L'idée selon laquelle les produits de dégradation de l'ApoE4 pourraient être toxiques a été évoquée », a déclaré Saghatelian. « Maintenant que nous connaissons l'enzyme qui les décompose, nous avons un moyen de tester cette hypothèse. »
Mais ce n'est pas seulement l'absence d'ApoE complète ou l'augmentation de ses fragments qui pourrait être à l'origine de la maladie d'Alzheimer chez les personnes atteintes d'ApoE4. Saghatelian et Chu ont également découvert qu'ApoE4, grâce à sa forte liaison à HtrA1, empêche l'enzyme de dégrader la protéine tau, responsable des enchevêtrements de tau associés à la maladie d'Alzheimer.
« Les gens ont pensé que la protéine tau ou la protéine bêta-amyloïde étaient responsables de la maladie d’Alzheimer, mais cela suggère que nous devons réfléchir de manière plus globale aux protéines qui pourraient avoir un impact sur la protéine tau ou la protéine amyloïde par le biais de voies biochimiques », a déclaré Saghatelian.
Ces résultats doivent être testés et confirmés par des études animales avant que les chercheurs puissent affirmer avec certitude que HtrA1 est le lien entre ApoE4 et la maladie d'Alzheimer chez l'homme. S'ils se confirment, ils pourraient ouvrir la voie à une meilleure compréhension de la maladie et à de nouvelles stratégies thérapeutiques potentielles.
Les autres chercheurs ayant participé à l’étude étaient Jolene K. Diedrich, Joan M. Vaughan, Cynthia J. Donaldson, Michael F. Nunn et Kuo-Fen Lee du Salk Institute.
Les travaux et les chercheurs impliqués ont été soutenus par des subventions du National Institutes of Health, le Fondation Clayton, le Fondation Schlink, la Fondation de la famille Gemcon, la bourse Hewitt, la Fondation Joe W. et Dorothy Dorsett Brown, la chaire Helen McLoraine en neurobiologie moléculaire, le National Cancer Center et le Leona M. et Harry B. Helmsley Charitable Trust.
BLOG
Journal de l'American Chemical Society
AUTEURS
Qian Chu, Jolene K. Diedrich, Joan M. Vaughan, Cynthia J. Donaldson, Michael F. Nunn, Kuo-Fen Lee et Alan Saghatelian
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.