
23 mai 2013
Les résultats surprenants des chercheurs de Salk laissent espérer que la thérapie actuellement testée dans le cancer avancé pourrait stopper la progression des cellules prémalignes.
Les résultats surprenants des chercheurs de Salk laissent espérer que la thérapie actuellement testée dans le cancer avancé pourrait stopper la progression des cellules prémalignes.
LA JOLLA, CA — Des scientifiques ont découvert un mécanisme de survie qui se produit dans les cellules mammaires qui viennent de devenir prémalignes – des cellules à la frontière entre la normalité et le cancer – ce qui pourrait conduire à de nouvelles méthodes pour arrêter les tumeurs.
Dans leurs Cellule moléculaire étude, les chercheurs de l'Institut Salk rapportent qu'une protéine connue sous le nom de facteur de croissance transformant bêta (TGF-β), considérée comme un suppresseur de tumeur dans le développement précoce du cancer, peut en fait favoriser cancer une fois qu'une cellule dérive vers un état précancéreux.
Cette découverte, une surprise pour les chercheurs, soulève la possibilité alléchante qu’avec un nouveau traitement, certains cancers pourraient être évités avant même de se développer.

Fernando Lopez-Diaz et Beverly M. Emerson du laboratoire de biologie réglementaire de Salk.
Images : avec l'aimable autorisation du Salk Institute for Biological Studies
« Nos travaux suggèrent qu'il pourrait être possible d'arrêter le développement du cancer dans les cellules prémalignes, celles qui ne sont qu'à quelques divisions de la normale », explique l'auteur principal de l'étude, Fernando Lopez-Diaz, chercheur au Laboratoire de biologie réglementaire à Salk.
Des agents conçus pour inhiber le TGF-β sont déjà testés contre des cancers qui se sont déjà propagés, selon Beverly M. Emerson, professeure Salk, directrice du laboratoire et auteure principale de l'étude. « Cette étude offre à la fois des informations importantes sur le développement précoce du cancer et une nouvelle voie à explorer dans le traitement du cancer », déclare-t-elle. « Ce serait formidable qu'un seul agent puisse stopper à la fois le cancer avancé et le cancer en phase terminale. »
Les oncologues pourraient également utiliser leur découverte pour prédire si les cellules précancéreuses d'un patient sont vouées à se transformer en cancer à part entière, ajoute Emerson. « Toutes les cellules précancéreuses ne se transforment pas en cancer », précise-t-elle. « Nombre d'entre elles s'autodétruisent grâce à des mécanismes de protection cellulaire. Mais certaines se transformeront en tumeurs et, à ce stade, il est impossible de prédire lesquelles de ces cellules présentent un risque. »
Les molécules TGF-β sont des protéines sécrétées présentes dans la plupart des tissus humains. Elles jouent différents rôles biologiques, notamment le contrôle de la prolifération cellulaire et de l'inflammation, et la cicatrisation des plaies.
Le dogme dominant en recherche sur le cancer est que la signalisation du TGF-β empêche les cellules de se transformer en cancer, explique Lopez-Diaz. Les scientifiques ont également reconnu que les cellules cancéreuses qui « souhaitent » se propager apprennent à utiliser la fonction de cicatrisation du TGF-β pour se détacher d'une tumeur, ajoute-t-il.
Une autre protéine, la protéine P53, est un suppresseur de tumeur connu. Lors de la réponse au stress qui se produit lorsqu'une cellule devient cancéreuse et en réponse à la chimiothérapie, la protéine p53 tente de réparer les dommages à l'ADN et, en cas d'échec, elle ordonne la mort de la cellule. « La voie p53 doit être sabotée pour que les cellules deviennent cancéreuses », explique Lopez-Diaz. « Cela se produit lorsque son gène subit une mutation, si la protéine p53 est excessivement dégradée ou, moins connu, si sa biosynthèse est entravée. »
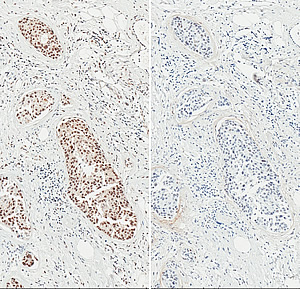
Cette image montre en marron l'activation de la signalisation TGFβ (à gauche) et des niveaux de p53 (à droite) lors d'une biopsie mammaire d'une patiente atteinte d'un carcinome canalaire in situ et invasif. Le TGFβ1 désactive la principale voie de signalisation régulant la réponse aux chimiothérapies et au stress cellulaire, suggérant une nouvelle thérapie potentielle pour prévenir la progression des cancers à un stade précoce et la résistance aux médicaments.
Images : avec l'aimable autorisation du Salk Institute for Biological Studies
Les chercheurs ont mené cette étude pour comprendre précisément comment p53 et TGF-β interagissent dans le développement du cancer. « Depuis une dizaine d'années, tout le monde pensait que ces deux voies interagissent dans les cellules normales et précancéreuses pour stopper le cancer, même si peu de données étayaient cette hypothèse », explique-t-il.
L'équipe a examiné des cellules prémalignes et cancéreuses provenant de tumeurs du sein et du poumon et a comparé des cellules mammaires normales et prémalignes provenant de femmes en bonne santé fournies par des scientifiques de l'Université de Californie à San Francisco.
Mais peu importe le nombre de façons différentes dont ils ont mené leurs expériences, les chercheurs de Salk ont découvert que le TGF-β peut interférer avec les réponses aux dommages cellulaires dans les cellules prémalignes ou cancéreuses.
En fait, ils ont découvert que le TGF-β arrête à la fois la transcription du gène p53 (le processus par lequel la machinerie cellulaire lit le code ADN d'un gène) et le processus ultérieur par lequel la protéine p53 correspondante est produite, connu sous le nom de traduction.
Cela pourrait expliquer pourquoi, dans environ la moitié des tumeurs mammaires, y compris les lésions précancéreuses, étudiées par l'équipe de l'UC San Francisco et du Sanford Burnham Medical Research Institute, lorsque la voie de signalisation TGF-β1 était fortement activée, les taux de p53 étaient réduits, et inversement : si la voie TGF-β1 était réduite, les taux de p53 étaient élevés. « Une tendance similaire a été observée avec PUMA, une protéine qui induit la mort cellulaire », ajoute Fernando Lopez-Diaz. « La protéine PUMA était plutôt abondante lorsque l'activation de TGF-β1 était faible, et inversement. »
« Le mauvais côté du TGF-β est apparu à quelques divisions cellulaires de la normalité, permettant aux cellules d’éviter la mort », explique-t-il.
Cette nouvelle immortalité explique de nombreux mystères oncologiques, explique Lopez-Diaz. « L'un d'eux est qu'elle éclaire la capacité des cellules cancéreuses prémalignes et précoces à résister à la chimiothérapie et aux autres traitements », ajoute-t-il.
Cela pourrait expliquer pourquoi 77 % des cancers du sein ont un gène p53 normal, et cela suggère en outre une manière dont les cellules cancéreuses peuvent utiliser les deux pour métastaser et survivre au voyage vers les organes où elles s'installent dans un nouveau foyer.
« Parce qu’il aide les cellules à éviter la mort, le TGF-β peut réduire l’impact négatif du processus métastatique sur les cellules cancéreuses », explique Lopez-Diaz.
Il ajoute qu'il reste encore beaucoup à faire. « Nous voulons comprendre les signaux qui transforment le TGF-β en un ennemi », dit-il. « Si nous les connaissons, nous pourrions être capables d'inhiber ces signaux et de forcer les cellules endommagées à mourir, comme elles le devraient. Cela pourrait nous offrir une autre possibilité de traitement, parallèlement aux inhibiteurs du TGF-β actuellement testés. »
Les autres auteurs de l'étude sont Sri Kripa Balakrishnan, de Salk ; Philippe Gascard, Jianxin Zhao et Thea D. Tlsty, de l'Université de Californie à San Francisco ; et Sonia V. del Rincon et Charles Spruck, du Sanford Burnham Medical Research Institute.
L'étude a été financée par des subventions du Institut national du cancer (U54CA143803), la Fondation médicale Chambers
et une subvention du Centre du cancer (P30 CA014195).
À propos du Salk Institute for Biological Studies :
Le Salk Institute for Biological Studies est l'un des principaux instituts de recherche fondamentale au monde. Des professeurs de renommée internationale y explorent des questions fondamentales des sciences de la vie dans un environnement unique, collaboratif et créatif. Axés à la fois sur la découverte et sur l'encadrement des futures générations de chercheurs, les scientifiques du Salk contribuent de manière révolutionnaire à notre compréhension du cancer, du vieillissement, de la maladie d'Alzheimer, du diabète et des maladies infectieuses en étudiant les neurosciences, la génétique, la biologie cellulaire et végétale, et les disciplines connexes.
Les réalisations de ses professeurs ont été récompensées par de nombreuses distinctions, dont des prix Nobel et des adhésions à l'Académie nationale des sciences. Fondé en 1960 par le Dr Jonas Salk, pionnier du vaccin contre la polio, l'Institut est une organisation indépendante à but non lucratif et un monument architectural.
BLOG
Cellule moléculaire
AUTEURS
Fernando J. Lopez-Diaz, Philippe Gascard, Sri Kripa Balakrishnan, Jianxin Zhao, Sonia Valle del Rincon, Charles Spruck, Thea D. Tlsty, Beverly M. Emerson
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu