
12 août 2021
Les scientifiques de Salk montrent comment le blocage des récepteurs opioïdes dans des neurones spécifiques peut restaurer la respiration lors d'une surdose
Les scientifiques de Salk montrent comment le blocage des récepteurs opioïdes dans des neurones spécifiques peut restaurer la respiration lors d'une surdose
LA JOLLA — On sait depuis longtemps que les décès par overdose d'opioïdes sont causés par des troubles respiratoires, mais le mécanisme par lequel ces médicaments inhibent la respiration était encore méconnu. Une nouvelle étude menée par des scientifiques de Salk a identifié un groupe de neurones du tronc cérébral jouant un rôle clé dans ce processus.
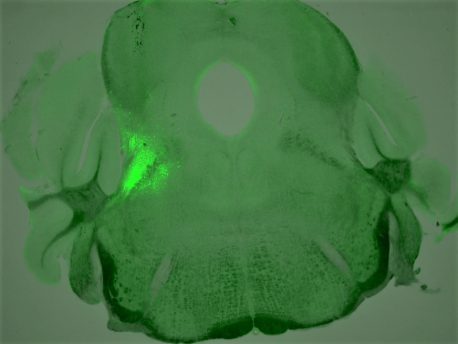
Les résultats, publiés le 8 juin 2021 dans la revue Actes de l'Académie nationale des sciences, montrent comment le déclenchement de récepteurs spécifiques dans ces neurones provoque une dépression respiratoire induite par les opioïdes (DROI), une perturbation respiratoire responsable des décès par overdose. L'étude montre également comment le blocage de ces récepteurs peut inverser la DROI.
« Le mécanisme sous-jacent expliquant pourquoi les opiacés ralentissent et dépriment le rythme respiratoire n'a pas été entièrement caractérisé », explique le chercheur principal. Han chanté, professeur adjoint aux Laboratoires de biologie des peptides de la Fondation Clayton de Salk. « Ces connaissances peuvent ouvrir la voie à de meilleures options thérapeutiques pour la maladie d'Alzheimer et des maladies apparentées. »
Aux États-Unis, plus de 93,000 2020 décès par overdose ont été enregistrés en 60, dont environ XNUMX % étaient imputables à des opioïdes comme le fentanyl. Les opioïdes agissent en se liant à des protéines des cellules nerveuses (neurones), appelées récepteurs opioïdes, inhibant ainsi leur activité. Actuellement, la naloxone est le seul médicament connu pour bloquer les effets des opioïdes et inverser une overdose. Cependant, la naloxone présente des limites, notamment sa courte durée d'action qui nécessite plusieurs administrations. Elle agit également de manière systémique, bloquant les récepteurs opioïdes dans tout l'organisme, y compris ceux qui contrôlent la douleur.
Afin de développer des stratégies plus spécifiques pour traiter la RIOI, l'équipe de Han a cherché à identifier les neurones respiratoires cérébraux porteurs de récepteurs opioïdes. Dans cette nouvelle étude, les chercheurs ont identifié un groupe de neurones exprimant un certain type de récepteur opioïde (le récepteur opioïde mu) et situés dans le centre de modulation respiratoire du tronc cérébral ; ils ont ensuite caractérisé le rôle de ces neurones dans la RIOI.
Ils ont constaté que les souris génétiquement modifiées pour être dépourvues de récepteurs opioïdes dans ces neurones ne présentaient pas de troubles respiratoires après exposition à la morphine, contrairement aux souris du groupe témoin. Les chercheurs ont également constaté que, sans introduction d'opioïdes, la stimulation de ces récepteurs chez les souris témoins provoquait des symptômes d'OIRD.

L’équipe a ensuite cherché des moyens d’inverser le processus en traitant les souris surdosées avec des composés chimiques ciblant d’autres récepteurs sur les mêmes neurones, qui jouent un rôle opposé à celui du récepteur opioïde (en les activant plutôt qu’en les inhibant).
« Nous avons découvert quatre composés chimiques différents qui ont activé ces neurones et rétabli le rythme respiratoire pendant l'OIRD », a déclaré Shijia Liu, auteur principal et étudiant diplômé du laboratoire Han. Le taux de récupération chez les souris surdosées était proche de 100 %, ce qui a surpris l'équipe.
Les chercheurs prévoient ensuite d'examiner si d'autres groupes cellulaires jouent également un rôle dans l'OIRD. Des études plus approfondies examineraient également le lien entre la régulation respiratoire et la perception de la douleur dans le cerveau, ouvrant ainsi la voie au développement de traitements plus ciblés pour l'OIRD.
« Nous espérons expliquer la ségrégation douleur-respiration au niveau moléculaire ou microcircuitique », explique Han, titulaire de la chaire de développement du Fonds Pioneer. « Ce faisant, nous pourrons tenter de rétablir la respiration sans modifier les effets analgésiques des opioïdes. »
Les autres auteurs de l'étude sont Dong-Il Kim, Tae Gyu Oh, Gerald M. Pao, Jong-Hyun Kim, Kuo Fen Lee et Ronald M. Evans de Salk ; Richard Palmiter de l'Université de Washington ; et Matthew R. Banghart de l'Université de Californie à San Diego.
La recherche a été soutenue par le National Institute of Mental Health, la Simons Foundation Autism Research Initiative, la Brain Research Foundation, la Klingenstein-Simons Fellowship Award in Neuroscience et la Rita Allen Foundation.
DOI: 10.1073 / pnas.2022134118
BLOG
Actes de l'Académie nationale des sciences
AUTEURS
Shijia Liu, Dong-Il Kim, Tae Gyu Oh, Gerald M. Pao, Jong-Hyun Kim, Richard D. Palmiter, Matthew R. Banghart, Kuo-Fen Lee, Ronald M. Evans et Sung Han
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.