
le 21 avril 2022
L'étude Salk pointe vers une nouvelle cible thérapeutique potentielle pour la pancréatite et le cancer du pancréas
L'étude Salk pointe vers une nouvelle cible thérapeutique potentielle pour la pancréatite et le cancer du pancréas
LA JOLLA — Chaque jour, votre pancréas produit environ une tasse de sucs digestifs, un mélange de molécules capables de décomposer les aliments que vous consommez. Mais si ces puissantes molécules sont activées avant d'atteindre l'intestin, elles peuvent endommager le pancréas lui-même, digérant les cellules qui les ont créées, provoquant une inflammation douloureuse appelée pancréatite et prédisposant au cancer du pancréas.
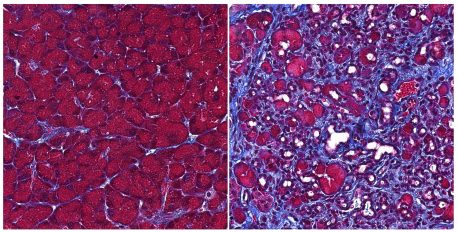
Maintenant, les scientifiques de Salk rapportent dans la revue Gastroentérologie Le 21 avril 2022, ils ont découvert qu'une protéine appelée récepteur gamma lié aux œstrogènes (ERR ɣ) est essentielle à la prévention de l'autodigestion pancréatique chez la souris. De plus, ils ont découvert que les personnes atteintes de pancréatite présentent des taux plus faibles d'ERR ɣ dans les cellules affectées par cette inflammation.
Ces résultats suggèrent que de nouvelles thérapies visant à réguler l’activité ERR ɣ pourraient aider à prévenir ou à traiter la pancréatite et le cancer du pancréas.
« Notre découverte apporte un nouvel éclairage sur la biologie fondamentale du fonctionnement des cellules du pancréas et sur les facteurs susceptibles de provoquer une pancréatite et un cancer du pancréas », explique le professeur Ronald Evans, directeur du laboratoire d'expression génétique de Salk, titulaire de la chaire March of Dimes en biologie moléculaire et développementale et co-auteur principal de l'étude.
Le pancréas abrite deux principaux types de cellules aux fonctions distinctes : les cellules bêta, qui libèrent de l'insuline pour réguler la glycémie, et les cellules acineuses, qui produisent les sucs digestifs. Evans et ses collègues découvert précédemment que l'ERR ɣ aide les cellules bêta pancréatiques à libérer de l'insuline et pourrait être utile dans le traitement du diabète. Lors d'études de suivi, l'équipe a également découvert que des souris dépourvues d'ERR ɣ développaient une pancréatite sévère.
Pour comprendre le rôle de l'ERR ɣ dans les cellules acineuses pancréatiques, les chercheurs ont comparé des souris, ainsi que des cellules isolées, avec et sans cette protéine. Ils ont découvert que l'ERR ɣ est nécessaire au fonctionnement des mitochondries des cellules acineuses, organites productrices d'énergie.

« On sait depuis les années 1960 que les mitochondries sont la principale source d’énergie des cellules acineuses, mais le facteur qui contrôle ce programme vital de production d’énergie dans les cellules acineuses est un mystère de longue date », explique le co-auteur principal Jae Myoung Suh de l’Institut coréen avancé des sciences et technologies (KAIST), en Corée du Sud.
Sans ERR ɣ, les cellules acineuses ont non seulement une régulation énergétique dysrégulée mais, par conséquent, activent de manière incorrecte les enzymes digestives pour démarrer l'autodigestion.
« Les mitochondries de ces cellules doivent être particulièrement robustes », explique Michael Downes, scientifique et co-auteur de la nouvelle étude. « En cas de problème, ces enzymes digestives sont activées, ce qui déclenche l'autodigestion du pancréas. »
Le groupe a montré que non seulement l’autodigestion des cellules acineuses pancréatiques commençait en l’absence d’ERR ɣ, mais que des changements cellulaires indiquant un cancer précoce du pancréas commençaient également.
Les chercheurs ont ensuite analysé les données de patients atteints de pancréatite afin de déterminer si les résultats obtenus chez la souris et en laboratoire étaient pertinents pour la maladie humaine. Ils ont comparé les biopsies de pancréatite à celles prélevées sur des cellules pancréatiques normales, y compris des sections saines du pancréas chez les mêmes patients. Ils ont découvert que les cellules atteintes de pancréatite présentaient des taux d'ERR ɣ plus faibles.
« Nous avons examiné les données de plusieurs endroits et groupes de patients différents et avons constaté que l'ERR ɣ diminue de manière très constante avec la pancréatite », explique le co-premier auteur Tae Gyu Oh, analyste bioinformatique chez Salk.

Oh et ses collègues ont ensuite montré que les niveaux de 83 autres gènes, dont beaucoup sont directement régulés par ERR ɣ, étaient également altérés dans les échantillons de pancréatite. De plus, en examinant les données de deux grandes études comparant l'expression génétique chez l'homme, ils ont découvert que certains de ces 83 gènes sont associés à des formes rares de pancréatite héréditaire et de cancer du pancréas.
« Le fait que cela ait été lié à des patients atteints de pancréatite chronique suggère que l’ERR ɣ est cliniquement pertinent et pourrait constituer une bonne cible médicamenteuse à l’avenir », explique Evans.
Les chercheurs prévoient de futures études pour examiner en profondeur les changements précancéreux auxquels conduisent la dysrégulation de l’ERR ɣ et la pancréatite, ainsi que la manière dont les médicaments pourraient aider à augmenter l’ERR ɣ pour prévenir ou traiter les maladies pancréatiques.
Français Les autres auteurs incluent Weiwei Fan, Sagar P. Bapat, Ye Zheng, Ruth T. Yu, Annette Atkins et Eiji Yoshihara de Salk ; Jinhyuk Choi, Heewon Jung, Kun-Young Park, Hyemi Shin, Taehee Jo, Du-Seock Kang, Sujung Hong et Pilhan Kim de KAIST ; Dipanjan Chanda et In-Kyu Lee de l'hôpital universitaire national de Kyungpook ; Jina Kim et Sung Jin Cho de la Fondation pour l'innovation médicale de Daegu-Gyeongbuk ; Moongi Ji et Man-Jeong Paik de l'université nationale de Sunchon ; Minkyo Jung et Ji Young Mun de l'Institut coréen de recherche sur le cerveau ; Takashi Syoji de l'université de Kyoto ; Ayami Matsushima de l'université de Kyushu ; David C. Whitcomb, Phil Greer et Brandon Blobner de l'université de Pittsburgh ; Mark O. Goodarzi et Stephen J. Pandol du centre médical Cedars-Sinai ; Jerome I. Rotter de l'UCLA ; Christopher Liddle de l'université de Sydney ; ainsi que l'ensemble du consortium North American Pancreatitis Study 2 (NAPS2).
Le travail a été financé en partie par le National Institute of Diabetes and Digestive and Kidney Diseases (T32 DK063922-17, NIH DK061451 et R01DK120480), le National Center for Research Resources (UL1 RR024153 et UL1TR000005), le NIH Roadmap for Medical Research, le Howard Hughes Medical Institute, la Lustgarten Foundation, la NOMIS Foundation, le SWCRF Investigator Award, la David C. Copley Foundation et la Don and Lorraine Freeberg Foundation.
DOI: 10.1053/j.gastro.2022.04.013
BLOG
Gastroentérologie
AUTEURS
Jinhyuk Choi, Tae Gyu Oh, Heewon Jung, Kun-Young Park, Hyemi Shin, Taehee Jo, Du-Seock Kang, Dipanjan Chanda, Sujung Hong, Jina Kim, Moongi Ji, Minkyo Jung, Takashi Syoji, Ayami Matsushima, Pilhan Kim, Ji Young Mun, Man-Jeong Paik, Sung Jin Cho, In-Kyu Lee, David C. Whitcomb, Phil Greer, Brandon Blobner, Mark O. Goodarzi, Stephen J. Pandol, Jerome I. Rotter, consortium North American Pancreatitis Study 2 (NAPS2), Weiwei Fan, Sagar P. Bapat, Ye Zheng, Christopher Liddle, Ruth T. Yu, Annette Atkins, Michael Downes, Eiji Yoshihara, Ronald M. Evans et Jae Myoung Suh
Bureau des communications
Tél: (858) 453-4100
presse@salk.edu
L’Institut Salk est un institut de recherche indépendant à but non lucratif, fondé en 1960 par Jonas Salk, inventeur du premier vaccin antipoliomyélitique sûr et efficace. Sa mission est de mener des recherches fondamentales, collaboratives et audacieuses pour relever les défis les plus urgents de la société, tels que le cancer, la maladie d’Alzheimer et la vulnérabilité de l’agriculture. Ces travaux scientifiques fondamentaux sous-tendent tous les efforts de recherche translationnelle, générant des connaissances qui permettent la mise au point de nouveaux médicaments et des innovations à l’échelle mondiale.