Vice-président, directeur scientifique
Professeur
Laboratoire de biologie moléculaire et cellulaire
Président Donald et Darlene Shiley

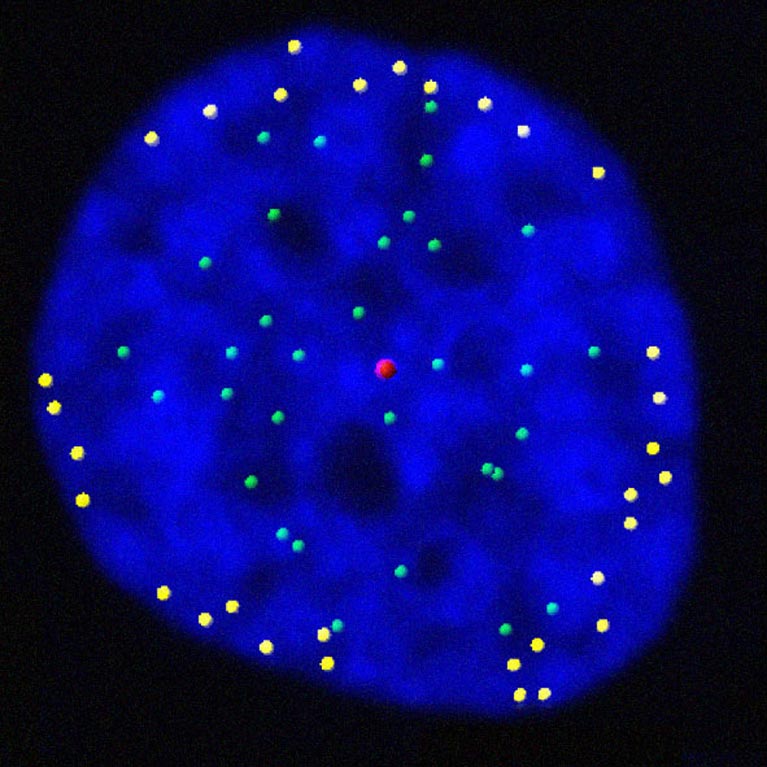
De même que chaque photocopie d'une copie devient un peu moins nette que la précédente, chaque fois qu'une cellule copie son matériel génétique, elle perd des détails aux extrémités de chaque chromosome. Ces extrémités, appelées télomères, finissent par s'éroder et exposent les gènes vitaux à l'usure, empêchant la cellule de croître ou provoquant sa mort. Les télomères régulent d'importantes limites prolifératives et limitent le potentiel de croissance cellulaire, inhibant ainsi la formation de cancers.
Cependant, dans de nombreuses cellules cancéreuses, les télomères se reconstruisent constamment, conférant ainsi à la cellule son immortalité. De même, la capacité de la cellule à réparer l'ADN endommagé diminue avec l'âge, entraînant l'accumulation de mutations et de maladies liées à l'âge. Si les scientifiques parviennent à déterminer comment stopper cette extension des télomères et améliorer la réparation de l'ADN au cours du vieillissement, ils pourraient provoquer la mort des cellules cancéreuses ou les rendre plus sensibles aux médicaments. À l'inverse, préserver l'intégrité des télomères et améliorer la réparation de l'ADN pourrait permettre de traiter les syndromes de vieillissement prématuré. Mais les chercheurs doivent d'abord comprendre les tenants et aboutissants complexes du fonctionnement normal des télomères et de la régulation de la réparation de l'ADN.
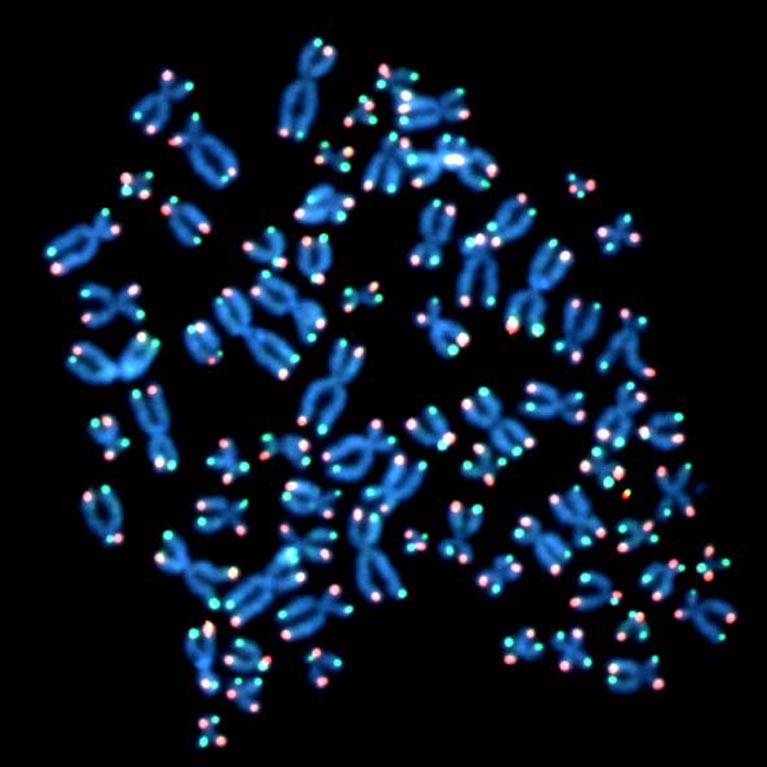
Jan Karlseder étudie le rôle des télomères tout au long du cycle prolifératif d'une cellule, depuis le moment où la cellule commence à copier son matériel génétique jusqu'au moment où elle se divise en deux nouvelles cellules, ainsi que tout au long de la vie de la cellule, depuis le moment où une jeune cellule émerge par division cellulaire jusqu'au moment où une vieille cellule se « retire » définitivement (devient sénescente) ou meurt.
Les limites de la division cellulaire, telles que celles fixées par le raccourcissement des télomères, sont essentielles pour limiter la division cellulaire incontrôlée et ainsi prévenir la formation de cancers. Les deux limites fondamentales empêchant les cellules humaines primaires de devenir cancéreuses sont : la sénescence réplicative, une forme de retraite cellulaire au cours de laquelle les cellules cessent de se diviser, et la crise, un état conduisant à la mort cellulaire. Si ces limites étaient reconnues depuis des décennies, on ignorait encore comment les cellules deviennent sénescentes et ce qui se passe lorsque les cellules continuent de se diviser alors qu'elles devraient sénescencer.
En découvrant et en définissant clairement les mécanismes régulant la division cellulaire des cellules humaines primaires (cellules prélevées sur des tissus vivants tels qu'une biopsie), le laboratoire Karlseder a exposé de nouvelles voies au cours des premiers stades de la formation du cancer, qui peuvent donner lieu à des interventions potentielles.
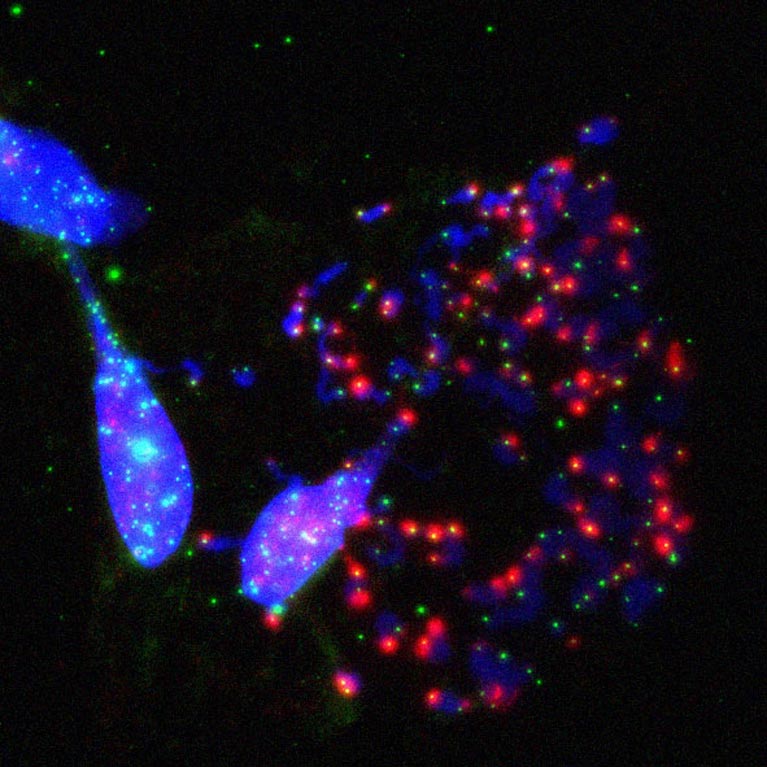
Le laboratoire de Karlseder a découvert que la mort cellulaire en cas de crise est exécutée par la machinerie de macroautophagie, un mécanisme de recyclage cellulaire, révélant une nouvelle voie suppressive de tumeur.
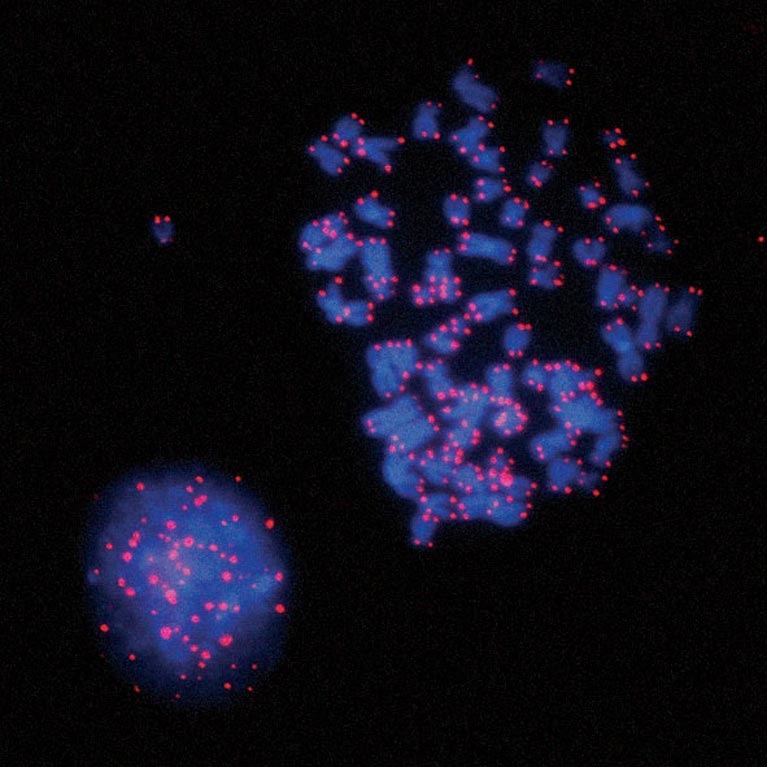
Lors du contournement de la sénescence, les télomères se raccourcissent davantage, jusqu'à la fusion des chromosomes. Karlseder et son équipe ont découvert que ces télomères fusionnés activent un point de contrôle cellulaire (assemblage du fuseau mitotique) qui provoque l'arrêt de la division cellulaire mitotique, au cours duquel le signal de dommage est amplifié et provoque la mort cellulaire en un seul cycle cellulaire.
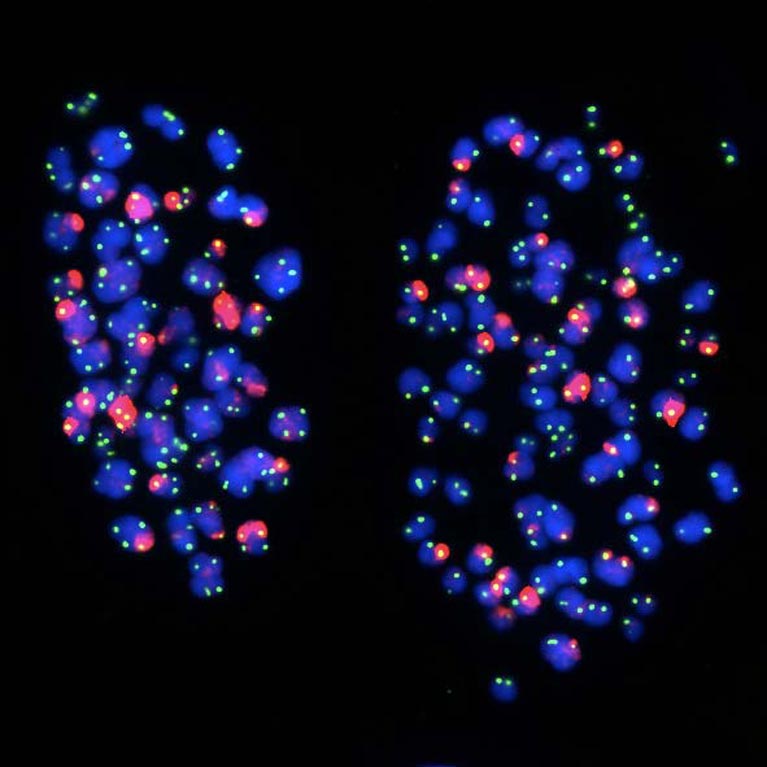
Son laboratoire a découvert que les télomères se déplacent vers la périphérie du noyau cellulaire après leur duplication. Ces résultats révèlent comment nos gènes sont régulés et comment les programmes d'expression génétique sont modifiés lors de la division cellulaire, une étape importante pour comprendre le vieillissement et les maladies liées à des mutations génétiques, comme le cancer.
Licence en biologie, Université d'Innsbruck, Autriche
Doctorat en biologie moléculaire, Université de Vienne
Bourse postdoctorale, Université Rockefeller, New York