
2020 년 1 월 21 일
이전에 연구된 두 가지 골관절염 약물의 조합이 약물 단독보다 더 효과적이라고 Salk 연구원이 발견했습니다.
이전에 연구된 두 가지 골관절염 약물의 조합이 약물 단독보다 더 효과적이라고 Salk 연구원이 발견했습니다.
LA JOLLA—골관절염 또는 "마모" 관절염이 있는 사람들은 진통제 또는 관절 교체 수술과 같은 치료 옵션이 제한적입니다. 이제 Salk 연구원들은 두 가지 실험 약물의 강력한 조합이 고립된 인간 연골 세포뿐만 아니라 쥐의 골관절염의 세포 및 분자 징후를 역전시킨다는 것을 발견했습니다. 그들의 결과는 저널에 게재되었습니다. 단백질 및 세포 1월 16, 2020합니다.
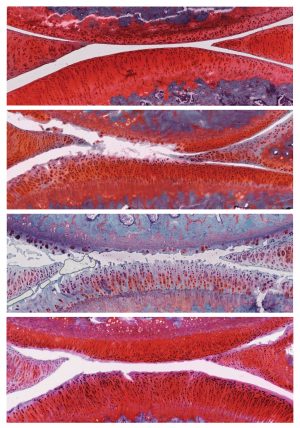
더 알아보기 고해상도 이미지를 위해.
신용: 소크 연구소
"정말 흥미로운 점은 이것이 잠재적으로 매우 쉽게 클리닉으로 전환될 수 있는 치료법이라는 것입니다."라고 말합니다. 후안 카를로스 이즈피수아 벨몬테, Salk 유전자 발현 연구소의 수석 저자이자 교수입니다. "우리는 인간 사용을 위해 이 유망한 조합 요법을 계속 개선하게 되어 기쁩니다."
30천만 명의 성인에게 영향을 미치는 골관절염은 미국에서 가장 흔한 관절 장애이며 인구 고령화와 비만율 증가로 인해 향후 몇 년 동안 유병률이 증가할 것으로 예상됩니다. 이 질병은 뼈와 관절을 보호하는 연골의 점진적인 변화로 인해 발생합니다. 노화와 반복적인 스트레스를 받으면 이 관절 연골 세포의 분자와 유전자가 변해 결국 연골이 파괴되고 기저 뼈가 과성장해 만성 통증과 경직을 일으킨다.
이전 연구에서는 골관절염을 치료할 수 있는 잠재적 약물로 알파-KLOTHO와 TGFβR2(TGFβR2)라는 두 분자를 정확히 지적했습니다. αKLOTHO는 관절 연골 세포를 둘러싼 분자 망에 작용하여 이 세포 외 기질이 분해되는 것을 방지합니다. TGFβR2는 연골 세포에 보다 직접적으로 작용하여 연골 세포의 증식을 촉진하고 손상을 방지합니다.
각각의 약물만으로 질병의 동물 모델에서 골관절염을 적당히 억제했지만 Izpisua Belmonte와 그의 동료들은 두 약물이 함께 사용하면 더 효과적으로 작용할 수 있을지 궁금해했습니다.
"우리는 서로 다른 방식으로 작동하는 이 두 분자를 혼합함으로써 더 나은 것을 만들 수 있을 것이라고 생각했습니다.
연구자들은 αKLOTHO와 TGFβR2를 만들기 위한 DNA 지침을 포함하는 바이러스 입자로 골관절염이 있는 젊고 건강한 쥐를 치료했습니다.
치료 2주 후 대조군 입자를 투여한 쥐는 무릎에 더 심각한 골관절염이 있었고 질병은 4단계에서 2단계로 진행되었습니다. 그러나 αKLOTHO 및 TGFβR2 DNA가 포함된 입자를 투여받은 쥐는 연골이 회복되었습니다. 연골은 더 두꺼웠고, 더 적은 수의 세포가 사멸했으며, 활발하게 증식하는 세포가 존재했습니다. 이 동물의 질병은 가벼운 형태의 골관절염인 1단계에서 XNUMX단계로 호전되었으며 부정적인 부작용은 관찰되지 않았습니다.

더 알아보기 고해상도 이미지를 위해.
신용: 소크 연구소
Salk 박사후 연구원이자 이 논문의 공동 제XNUMX저자인 Isabel Guillen-Guillen은 "처음 몇 마리의 동물에게 이 약물 조합을 테스트했을 때부터 엄청난 개선을 보았습니다."라고 말했습니다. "우리는 더 많은 동물을 계속 확인했고 동일한 고무적인 결과를 보았습니다."
추가 실험에서 대조군 쥐에 비해 처리된 쥐의 연골 세포에서 더 활성화된 136개의 유전자와 덜 활성화된 18개의 유전자가 밝혀졌습니다. 그 중에는 염증과 면역 반응에 관여하는 유전자가 있어 병용 치료가 작동하는 일부 경로를 시사합니다.
인간에 대한 약물 조합의 적용 가능성을 테스트하기 위해 팀은 분리된 인간 관절 연골 세포를 αKLOTHO 및 TGFβR2로 처리했습니다. 세포 증식, 세포 외 기질 형성 및 연골 세포 동일성에 관여하는 분자의 수준이 모두 증가했습니다.
Martinez-Redondo는 "이 약물이 인간의 무릎 관절에 어떤 영향을 미치는지 보여주는 것과는 다르지만 잠재적으로 환자에게 효과가 있을 수 있다는 좋은 신호라고 생각합니다."라고 말합니다.
연구팀은 αKLOTHO와 TGFβR2 단백질의 용해성 분자를 바이러스 입자를 통해 투여하지 않고 직접 섭취할 수 있는지를 조사하는 등 치료제를 추가로 개발할 계획이다. 그들은 또한 증상이 나타나기 전에 약물 조합이 골관절염의 발병을 예방할 수 있는지 여부를 연구할 것입니다.
"우리는 이것이 인간의 골관절염에 대한 실행 가능한 치료법이 될 수 있다고 생각합니다."라고 Clinica CEMTRO의 책임자이자 공동 교신 저자인 Pedro Guillen은 말했습니다.
다른 저자로는 Chao Wang, Javier Prieto, Masakazu Kurita, Fumiyuki Hatanaka, Cuiqing Zhong, Reyna Hernandez-Benitez, Tomoaki Hishida, Takashi Lezaki, Akihisa Sakamoto, Amy Nemeth, Yuriko Hishida, Concepcion Rodriguez Esteban, Kensaku Shojima, Pradeep Reddy, Ling Huang이 있습니다. Salk의 Maxim Shokhirev; Noah Davidson과 Harvard University의 George Church; Universidad Católica San Antonio de Murcia의 Estrella Nuñez-Delicado; 바르셀로나 병원 클리닉의 Josep Campistol; Clinica CEMTRO의 Isabel Guillen-Vicente, Elena Rodriguez-Iñigo, Juan Manuel Lopez-Alcorocho, Marta Guillen-Vicente 및 Pedro Guillen-Garcia; 중국과학원의 Guang-Hui Liu.
일지
단백질 및 세포
작가
Paloma Martinez-Redondo, Isabel Guillen-Guillen, Noah Davidsohn, Chao Wang, Javier Prieto, Masakazu Kurita, Fumiyuki Hatanaka, Cuiqing Zhong, Reyna Hernandez-Benitez, Tomoaki Hishida, Takashi Lezaki, Akihisa Sakamoto, Amy N. Nemeth, Yuriko Hishida, Concepcion Rodriguez Esteban, Kensaku Shojima, Ling Huang, Maxim Shokhirev, Estrella Nuñez-Delicado, Josep M. Campistol, Isabel Guillen-Vicente, Elena Rodriguez-Iñigo, Juan Manuel Lopez-Alcorocho, Marta Guillen-Vicente, George Church, Pradeep Reddy, Pedro Guillen-Garcia, Guang-Hui Liu, 후안 카를로스 이즈피수아 벨몬테
커뮤니케이션 사무소
전화 : (858) 453-4100
press@salk.edu
솔크 연구소는 최초의 안전하고 효과적인 소아마비 백신 개발자인 조너스 솔크가 1960년에 설립한 독립적인 비영리 연구 기관입니다. 연구소의 사명은 암, 알츠하이머병, 농업 취약성 등 사회가 직면한 가장 시급한 문제들을 해결하기 위한 기초적이고 협력적이며 과감한 연구를 추진하는 것입니다. 이러한 기초 과학은 모든 응용 연구의 기반이 되어 전 세계적으로 새로운 의약품과 혁신을 가능하게 하는 통찰력을 제공합니다.