
7 декабря 2015
Команда Солка идентифицировала лекарство, которое предотвращает и устраняет смертельное повреждение печени у мышей
Команда Солка идентифицировала лекарство, которое предотвращает и устраняет смертельное повреждение печени у мышей
LA JOLLA — Хроническое повреждение печени в конечном итоге приводит к образованию раны, которая никогда не заживает. Это состояние, называемое фиброзом, постепенно заменяет нормальные клетки печени, которые обезвреживают пищу и жидкость, которые мы потребляем, все большим и большим количеством рубцовой ткани, пока орган не перестанет работать.
Ученые из Института Солка нашли лекарство, которое останавливает неконтролируемое накопление рубцовой ткани в печени. Небольшая молекула, названная JQ1, предотвращает, а также обращает вспять фиброз у животных и может помочь миллионам людей во всем мире, страдающим от фиброза и цирроза печени, вызванных алкоголизмом и такими заболеваниями, как гепатит. Эти результаты были опубликованы в PNAS на неделе 7 декабря 2015 г.
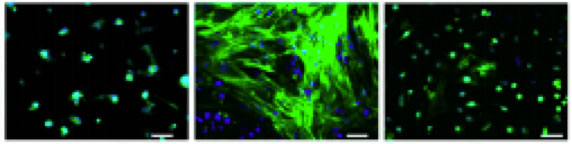
Предоставлено: Институт биологических исследований Солка.
«После слишком большого повреждения печени сама рубцовая ткань вызывает еще больше рубцовой ткани», — говорит Рональд Эванс, профессор и директор Лаборатории экспрессии генов Солка и исследователь Медицинского института Говарда Хьюза. «Мы действительно можем обратить вспять фиброз печени у животных и сейчас изучаем потенциальные терапевтические применения для людей».
При повреждении печени к ране призываются небольшие скопления печеночных звездчатых клеток, специализирующихся на запасании витамина А. Эти активированные звездчатые клетки выделяют витамин А, перемещаются к месту повреждения и создают толстую волокнистую рубцовую ткань, чтобы отгораживать и восстанавливать повреждения. Однако при длительном органном стрессе здоровые клетки печени замещаются рубцовой тканью, что в конечном итоге приводит к органной недостаточности.
«Традиционные методы лечения воспаления не работают, потому что у этих клеток есть несколько способов обойти лекарство», — говорит Майкл Даунс, старший научный сотрудник Солка и автор статьи. «Напротив, наша стратегия заключалась в том, чтобы остановить фиброзную реакцию на уровне генома, где сходятся эти пути».
Поиск критического пути генома стал золотым, обнаружив регуляторный белок, называемый BRD4, который является основным регулятором фиброза печени.

Нажмите здесь, чтобы увидеть изображение с высоким разрешением»
Изображение: предоставлено Институтом биологических исследований Солка.
Имея в руках эти новые знания, команда Солка обнаружила, что JQ1 успешно ингибирует BRD4 и останавливает трансформацию звездчатых клеток печени в клетки, продуцирующие волокна. Это хорошая новость, поскольку JQ1 является прототипом нового класса лекарств, которые в настоящее время проходят клинические испытания на людях при различных видах рака.
«JQ1 не только защищает от раневой реакции, но и обращает фиброзную реакцию у мышей», — говорит Рут Ю, научный сотрудник Солка и один из авторов статьи.
«Наши результаты показывают, что BRD4 является движущей силой хронического фиброза и многообещающей терапевтической мишенью для лечения заболеваний печени», — говорит Эванс, который также возглавляет кафедру молекулярной биологии и биологии развития March of Dimes. «Мы считаем, что это открытие может также лечить фиброз в других органах, таких как легкие, поджелудочная железа и почки».
Среди других авторов Нин Дин, Насун Ха, Мара Шерман, Крис Беннер, Матиас Леблан и Минсяо Хе из Института Солка, а также Кристофер Лиддл из Сиднейского университета.
Работа финансировалась NIH, Национальным советом по здравоохранению и медицинским исследованиям Австралии, благотворительным фондом Леоны М. и Гарри Б. Хелмсли, Фондом исследований рака Сэмюэля Ваксмана и Ipsen/Biomeasure.
ЖУРНАЛ
PNAS
АВТОРЫ
Нин Дин, Насун Ха, Рут Т. Ю, Мара Х. Шерман, Крис Беннер, Матиас Леблан, Минсяо Хэ, Кристофер Лиддл, Майкл Даунс и Рональд М. Эванс
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.